BioS+
-
"JPM 첫날" 애브비, 中 'VEGFxPD-1' 계약금 6.5억弗 빅딜
김성민 기자 2026-01-13 12:02
-
마드리갈, 화이자서 MASH 2상 ‘DGAT2 저해제’ 인수
이주연 기자 2026-01-13 11:30
-
머크, ‘B7-H3 ADC’ 소세포폐암 3상 “FDA 보류해제”
신창민 기자 2026-01-13 11:10
-
애로우헤드, 지방축적 타깃 'siRNA' 비만서 "초기 PoC"
김성민 기자 2026-01-13 09:56
-
에어넥시스, 시리즈A 2억弗..中서 PDE3/4 도입 "출범”
신창민 기자 2026-01-13 09:40
-
로슈, 中메디링크 ‘B7-H3 ADC’ 계약금 5.7억弗 "베팅"
이주연 기자 2026-01-13 07:11
-
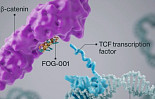
파라빌리스, 시리즈F 3.05억弗.."Wnt 타깃 펩타이드"
이주연 기자 2026-01-12 15:58
-
'RPT' 액티스, '새해 첫' 나스닥 IPO 3.18억弗 "흥행"
김성민 기자 2026-01-12 13:30
-
SK바이오팜, 225Ac 'NTSR1 RPT' 1상 "FDA 승인"
김성민 기자 2026-01-12 09:55
-
에피바이오, 시리즈B 1.07억弗..EGFR ‘이중항체 TPD’
신창민 기자 2026-01-12 09:25
-
릴리, '젭바운드+IL-17' 건선성관절염 3b상도 "성공"
이주연 기자 2026-01-12 07:24
-
알베우스, 비만 "분기투여" 'MariTide 전략' 1.6억弗 출범
김성민 기자 2026-01-09 12:46
-
GSK, ‘HBV ASO’ 만성B형간염 완치 3상 “히트”
신창민 기자 2026-01-09 09:58
-
알루미스, ‘TYK2 저해제' 건선 3상 "성공”..주가 115%↑
이주연 기자 2026-01-09 09:08
-
암젠, 'MLLT TPD' 다크블루 8.4억弗 인수.."메닌 한계극복"
김성민 기자 2026-01-09 07:03
-
한미약품, '벨바라페닙' NRAS 흑색종 "국내 2상 승인"
김성민 기자 2026-01-08 15:59























![[인사]대원제약, 2026년 정기 승진 인사](https://img.etoday.co.kr/crop/77/77/1956956.jpg)





![[인사]대원제약, 2026년 정기 승진 인사](https://img.etoday.co.kr/crop/74/74/1956956.jpg)