국제
사이넥시스, 칸디다 질염 3상 '성공'.."20년만의 신약 기대"
바이오스펙테이터 서일 기자
비(非) 아졸계 약물 ‘아이브렉사펀저프’, 치료 10일차에 칸디다 질염 증상과 징후 개선하며 1차 종결점 충족

사이넥시스(Scynexis)가 칸디다 질염(VVC)에 대한 새로운 경구용 치료제의 임상 3상에서 긍정적 결과를 얻었다. 만약 미국 식품의약국(FDA)에서 승인될 경우 20년만에 새 약물이 출시될 것이라고 회사는 기대했다.
사이넥시스는 21일(현지시간) 질 효모 감염증으로 알려진 칸디다 질염(vulvovaginal candidiasis, VVC)에 대한 광범위한(broad-spectrum) 경구용 항진균제 ‘아이브렉사펀저프(ibrexafungerp, IBX)’의 상업화 임상 3상(VANISH-306, NCT03987620)에서 1차∙2차 종결점을 충족시킨 결과를 발표했다.
사이넥시스는 2020년 하반기까지 미국 식품의약국(FDA)에 아이브렉사펀저프의 신약허가신청서(NDA)을 제출할 예정이다.
칸디다 질염은 칸디다 균으로 인한 질염으로 세균성 질염에 이어 두번째로 흔하게 발병한다. 칸디다 질염은 가려움증, 통증, 자극, 비정상적인 질 분비물 등의 증상을 보이며 성적 민감도 감소, 심리적 고통, 불임 등을 유발할 수 있다. 사이넥시스에 따르면 전 세계 여성의 약 75%는 일생동안 한번 이상, 40~50%는 두 번이상 칸디다 질염을 경험한다. 특히, 칸디다 질염 앓았던 여성의 약 6~8%는 재발성 질환으로 발전할 수 있다.
현재 칸디다 질염의 치료에는 ‘클로트리마졸(clotrimazole)’, ‘미코나졸(miconazole)’ 등의 아졸(azole) 항진균제(연고)를 사용한다. 미국에서 유일하게 승인된 경구용 항진균제인 플루코나졸(fluconazole)은 칸디다 질염에 55%의 치료효과를 보이며 태아에게 잠재적으로 치명적인 영향을 줄 수 있는 부작용이 있다. 플루코나졸에 내성을 보이는 칸디다 질염환자의 경우 경구용 치료제의 대안은 없으며 재발성 칸디다 질염의 예방을 위해 승인된 약물도 없는 상황이다.
사이넥시스에 따르면 아이브렉사펀저프는 항진균제(antifungal)로 글루칸 합성 저해제(glucan synthase inhibitor)로 ‘펀저프(fungerps)’ 계열의 첫 약물이다. 아졸계 약물과 구조가 달라 경구용 또는 정맥주사형으로 개발할 수 있다. 아이브렉사펀저프는 현재 칸디다(Canddida)와 아르페길러스(Aspergillus) 종에 의한 곰팡이 감염의 치료제로 개발 중이다.
발표에 따르면 사이넥시스는 칸디다 질염환자 188명을 2:1의 비율로 아이브렉사펀저프 투여군과 위약군으로 나눠서 VANISH-306 임상 3상을 진행했다. 사이넥시스는 10일차 병원에 방문(test-of-Cure, TOC)해 칸디다 질염의 증상과 징후를 평가한 결과를 1차 종결점으로 설정하고, 방문(TOC) 당시 균의 완전제거, 임상증상 개선, 25일차에 병원 방문 시 완치(complete symptom resolution)을 2차 종결점으로 삼아 평가했다.
사이넥시스는 칸디다 질염 환자들에게 아이브렉사펀저프를 300mg 용량으로 12시간에 한번씩 하루 두번 투여한 결과, 10일차 병원 방문(TOC)에서 63.3%(p<0.01)의 환자가 증상이 개선돼 위약군과 유의성있는 차이를 보이며 1차 종결점을 충족시켰다고 설명했다. 추가로 2차 종결점으로 설정한 균의 완전제거는 58.5%(p<0.01), 임상증상 개선은 72.3%(p<0.01), 25일차 완치는 73.9%(p<0.001)의 환자 비율을 나타냈다.
마르코 타글리티(Marco Taglietti) 사이넥시스 CEO는 “아이브렉사펀저프는 VVC에 대한 유일한 비(非) 아졸 치료제로, 칸디다 질염에 새로 승인된 치료제가 20년여동안 없던 상황이었다”며 “올해 말 미국 FDA에 신약허가신청(NDA)을 할 계획”이라고 말했다.
그는 이어 “VANISH 임상 3상에서 나타난 긍정적인 결과는 아이브렉사펀저프가 광범위한 칸디다질염을 해결해 줄 가능성과 동시에 기존 치료법에 반응하지 않는 환자들에게 새로운 치료법이 될 것이라 생각한다”고 덧붙였다.
한편, 사이넥시스는 VANISH-306 임상 결과가 이전에 진행한 아이브렉사펀저프 VANISH-303 임상 3상 결과와 일치하는 임상효과를 나타냈다고 설명했다. 사이넥시스는 현재 아이브렉사펀저프의 칸디다 질염 예방을 위한 CANDLE 임상 3상을 진행하고 있으며 2021년 하반기 탑라인 결과를 발표할 예정이다. 현재까지 VVC 예방에 대해 승인된 약물은 없는 상황이다.
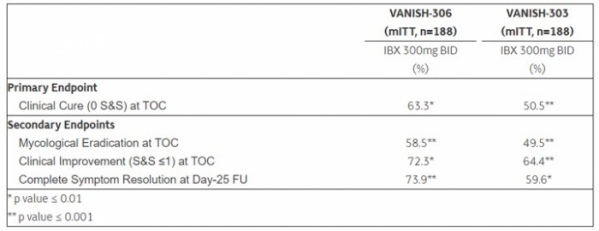
▲아이브렉사펀저프의 VANISH 임상 3상 결과(사이넥시스 보도자료)













![[BioS 레터]무균주사제 공급망 변화와 CDMO 대응](https://img.etoday.co.kr/crop/77/77/2262816.jpg)


