국제
AZ-머크, '린파자' mCRPC 3상서 “OS도 개선”
바이오스펙테이터 서일 기자
PARP 저해제 ‘린파자’, OS 개선하며 2차 종결점 충족..작년 동일 임상서 rPFS개선, 1차 종결점 충족

아스트라제네카(Astrazeneca)와 미국 머크(MSD)가 HHR 돌연변이를 가진 전이성 거세저항성 전립선암(mCRPC) 임상 3상에서 전체생존기간(OS)를 개선한 결과를 추가로 발표했다. 아스트라제네카와 머크는 지난해 8월 동일한 임상에서 방사선상 무진행생존기간(rPFS)를 개선한 결과를 밝힌 바 있다.
아스트라제네카와 머크는 지난 24일(현지시간) PARP 저해제 ‘린파자(Lynparza, olaparib)’가 HHR 돌연변이를 가진 전이성 거세저항성 전립선암(metastatic castration-resistant prostate cancer, mCRPC)을 대상으로 하는 PROfound 임상 3상(NCT02987543)에서 전체생존기간(overall survival, OS)을 개선시킨 긍정적인 추가 결과를 발표했다.
상동재조합 교정 유전자 돌연변이(homologous recombination repair gene mutation, HRRm)는 mCPRC환자의 약 2~30%에서 발생한다. HRR 유전자는 정상세포에서 손상된 DNA를 교정하는 역할을 하는데, HRR 유전자에 돌연변이가 생기면 비정상적인 세포성장을 유발해 암세포가 형성된다.
미국 암학회(American Cancer Society, ACS)에 따르면 매년 약 20만명이 새롭게 전립선암으로 진단받는다. 전립선 암에 사용하는 호르몬 요법인 안드로젠 억제 치료법(androgen suppression therapy)에 반응을 보이지 않으면 전이성 거세저항성 전립선암(mCRPC)라고 하며, 전체 전립선 암환자의 10~20%를 차지한다. mCRPC 환자의 평균 생존 기간은 2년 미만이다.
발표에 따르면 HRRm의 소집단(subpopulation)인 BRCA1/2 또는 ATM 유전자 돌연변이를 가진 mCRPC 환자 387명을 두그룹으로 나눠 ‘린파자’와 새로운 호르몬치료제(new hormonal agent, NHA)인 아스텔라스(Astellas)와 화이자(Pfizer)의 ‘엑스탄디(Xtandi, enzalutamide)’ 또는 존슨앤존슨(Johnson&Johnson)의 ‘자이티가(Zytiga, abiraterone acetate)’를 투여해 효과를 비교했다.
그 결과 린파자 투여군에서 경쟁약물 대비 전체 생존률(overall survival)을 통계적으로 유의미하고 임상적으로도 의미있게 개선하며 2차 종결점을 충족시켰다. 아스트라제네카과 머크는 지난해 8월, 동일 임상에서 린파자 투여군이 방사선학적 무진행생존기간(radiographic progression-free survival, rPFS)를 개선하며 1차 종결점을 충족시킨 결과를 발표한 바 있다. 린파자의 안전성과 내약성 프로파일은 이전 임상결과와 일관성을 보였다.
아스트라제네카와 머크는 추후 열릴 학회에서 PROfound 임상 3상의 결과를 정리해 발표할 계획이다.
조스 바셀가(Jose Baselga) 아스트라제네카 항암제 연구개발부 부사장은 “전이성 거세저항성 전립선암(mCRPC) 환자에서 보인 전체 생존기간의 개선은 도달하기 어려운 도전 과제였다”며 “린파자의 고무적인 결과를 바탕으로 규제기관과 협력해 가능한 빨리 환자들에게 제공할 수 있도록 할 것”이라고 말했다.
로이 베인스(Roy baynes) 머크 부사장은 “린파자는 BRCA 또는 ATM 돌연변이를 가진 mCRPC환자의 전체생존기간과 무진행생존기간을 개선하는등 임상적 이점을 보여줬다”며 “린파자는 mCRPC환자의 치료 표준(treatment standard)를 바꿀 수 있는 잠재력을 보였다”고 말했다.
한편, 린파자는 지난 1월 HRRm mCRPC 환자를 대상으로 미국 식품의약국(FDA)에서 우선심사 대상으로 지정받았다. 아스트라제네카와 머크는 mCRPC 환자에 대한 1차 치료제 사용하기 위해 ‘린파자+자이티가’병용요법과 자이티가 단일요법을 비교하는 PROpel 임상 3상을 진행 중이다.
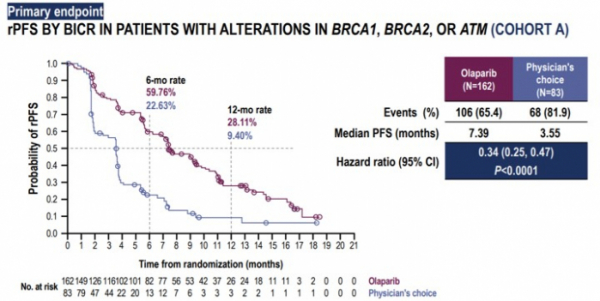
▲mCRPC 환자에서린파자 투여시 rPFS 증가 데이터(아스트라제네카, ESMO 2019 발표자료 참조)

















