국제
가미다셀, 혈액암 골수이식 3상.."호중구 생착시간 단축"
바이오스펙테이터 서일 기자
골수이식 세포치료제 ‘오미두비셀’..호중구 생착 시간 단축 1차 종결점 충족..2020년 4분기 BLA 제출예정

미국 바이오텍 가미다셀(Gamida cell)이 혈액암 치료를 위한 골수이식 세포치료제 임상 3상에서 호중구 생착(neutrophil engraftment) 시간을 단축시키며 1차 종결점을 충족시킨 탑라인 결과를 발표했다.
가미다셀은 12일(현지시간) 골수이식이 필요한 혈액암 환자들을 대상으로 진행한 세포치료제 ‘오미두비셀(omidubicel)’이 임상 3상에서 호중구 생착 시간을 단축시키며 1차 종결점을 충족시켰다고 밝혔다. 가미다셀은 2020년 4분기에 오미두비셀에 대한 생물의약품 허가신청서(BLA)를 미국 식품의약국(FDA)에 제출할 계획이다. 이 소식으로 가미다셀의 주가는 전일 대비 36.2%가 올랐다.
가미다셀은 호중구 생착이 골수이식을 받은 환자가 건강한 세포를 생산하기 시작하는지를 나타내는 척도로 호중구의 생착 속도가 빠르면 감염의 위험과 입원시간이 감소한다고 설명했다. 발표에 따르면 골수 이식 후 호중구 생착시간의 중간값은 오미두비셀 투여군에서 12일, 대조군에서 22일로 유의미한 차이를 보였다(p<0.001).
골수이식은 급성 백혈병 등의 혈액암을 앓고 있는 환자에게 완치를 목적으로 시행하는 치료법이다. 미국 보건복지부(HSS)에 따르면 골수이식으로 치료가 가능함에도 불구하고 약 40%의 환자는 기증자와 적합하지 않는 등의 이유로 이식을 받지 않는다. 대안으로 제대혈(cord blood)를 사용하지만, 줄기세포(stem cell)와 전구세포(progenitor cell)의 수가 적어 생착이 오래 걸리는 단점이 있었다. 이를 극복하기 위해 가미다셀은 제대혈에 니코틴아마이드(nicotinamide, NAM)를 사용해 줄기세포의 수를 늘리고 기능을 유지하는 아미두비셀을 개발했다.
미첼 홀로위츠(Mitchell Horwitz) 듀크암연구소 교수는 “새로운 골수이식 방식이 필요한 상황에서 오미두비셀이 보인 임상 3상 결과에 고무적이다”며 “생명이 위험한 혈액암 환자에게 줄기세포 이식을 더 성공적으로 할 수 있게 해주는 결과”라고 말했다. 이어 “생착 시간의 감소는 환자의 입원시간과 감염 가능성을 줄이기 때문에 임상적으로 의미가 있다”고 덧붙였다.
발표에 따르면 가미다셀은 125명의 혈액암 환자를 대조군 63명, 오미두비셀 투여군 62명으로 나눠 임상 3상(NCT02730299)을 진행했다. 혈액암 환자는 급성 림프구성백혈병(acute lymphoblastic leukemia), 급성 골수성백혈병(acute myelogenous leukemia), 만성 골수성백혈병(chronic myelogenous leukemia), 골수이형성 증후군(myelodysplastic syndrome) 등을 앓고 있었다.
가미다셀은 오미두비셀이 호중구 생착시간을 감소시키며 1차 종결점을 충족시켰다고 밝혔다. 구체적으로 오미두비셀의 호중구 생착시간의 중간값은 12일(95% CI: 10~15)로 대조군 22일(95% CI: 19~25)에 비해 짧았다. 호중구 생착에 성공한 비율은 오미두비셀을 투여받은 환자에서 96%로 대조군 88% 대비 높았다.
가미다셀은 올해 하반기에 개최될 학회에서 전체 결과를 분석해 발표할 예정이다.
줄리안 아담스(Julian Adams) 가미다셀 CEO는 “오미두비셀은 FDA에서 혁신의약품으로 지정받은 최초의 골수이식제품이면서 FDA가 승인한 첫 골수이식편(bone marrow transplant graft)이 될 가능성이 있다”며 “임상 3상의 결과에 고무돼 있으며, 올해 4분기 FDA에 생물의약품 허가신청서(BLA)를 제출할 예정”이라고 말했다.
한편, 가미다셀은 이번 결과가 임상 1/2상(NCT01816230) 결과와 일치한다고 설명했다. 가미다셀은 혈액암 환자 36명과 대조군 146명을 대상으로 진행한 임상 1/2상에서 오미두비셀로 치료받은 환자의 호중구 생착시간 중간값은 11.5일(95% CI: 9~14)로 대조군은 21일(95% CI: 20~23)에 비해 짧았다.
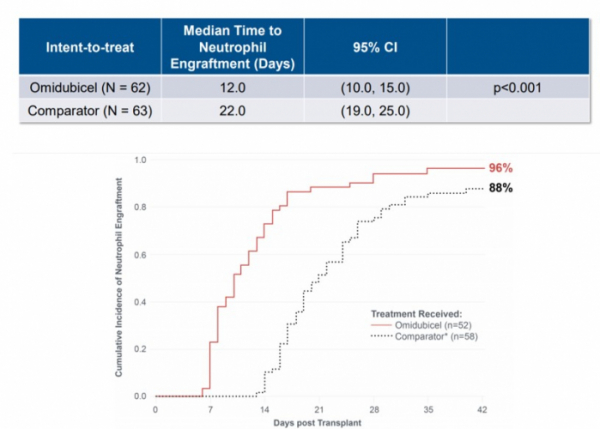
▲혈액암 환자에게 오미두비셀 투여후 생착시간과 생착비율(가미다셀 발표자료 참조)



















