기업
한미약품, 유럽간학회서 NASH신약 2a상 결과 공개
바이오스펙테이터 장종원 기자
Glucagon/GIP/GLP-1 삼중작용 'LAPSTriple Agonist'..최고 용량 투여 그룹서 지방간 평균 81.2% 감소
한미약품은 오는 27일 온라인으로 개최되는 유럽간학회 국제 간 학술대회(EASL ILC)에서 비알콜성 지방간염 치료제(NASH) 'LAPSTriple Agonist(HM15211)'의 임상(2a상) 및 전임상 연구 결과 3건을 발표한다고 18일 밝혔다.
먼저 한미약품은 LAPSTriple Agonist 임상 2a상 연구결과를 듀크대학교 마날 압델말렉(Manal Abdelmalek) 교수 발표로 공개한다.
앞서 공개한 연구에 따르면, NAFLD(비알코올성지방간)을 동반한 비만 환자 66명을 대상으로 LAPSTriple Agonist를 12주 반복 투여한 결과, 안전성과 내약성 및 지방간 감소 효능이 확인됐다. 특히 최고 용량 투여 그룹에서 투여 전 대비 지방간이 평균 81.2% 감소했으며, 모든 환자에서 지방간이 50% 이상 감소했다.
또 '지방간 30% 이상 감소 효과'가 저용량에서는 70% 이상 환자에서, 고용량에서는 모든 환자에서 확인됐다.
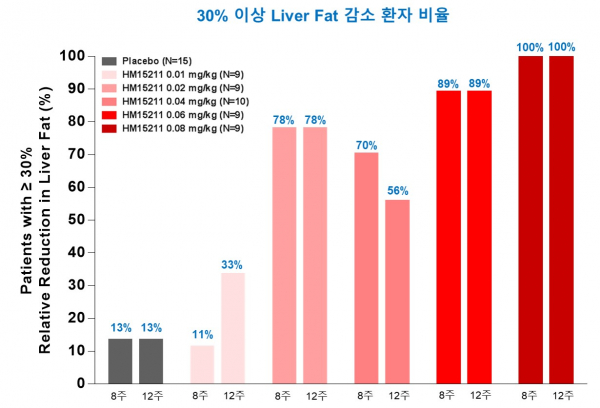
▲LAPSTriple Agonist 투여 전 대비 30% 이상 간 내 지방 감소를 보인 환자 비율. 한미약품 제공.
이번 연구결과는 학회의 Late Breaking Session 발표 대상으로 선정됐다. 유럽간학회는 임상 진행 상황 등으로 인해 정해진 기간 내 자료를 제출하지 못하더라도 해당 연구의 혁신성과 중요도가 인정되면 발표할 수 있는 기회를 부여하고 있다. LAPSTriple Agonist는 지난 7월 NASH 치료를 위한 미국 FDA의 패스트트랙(Fast Track) 프로그램으로도 지정된 바 있다.
이와 함께 한미약품은 건강한 비만 환자 41명 대상의 단회투여 글로벌 임상 1상에서 지방간과 간염증, 간 섬유화를 복합적으로 표적하는 LAPSTriple Agonist의 안전성과 내약성을 확인한 연구 결과도 포스터로 발표한다.
또 한미약품은 NASH 및 간 섬유화, 담즙 정체성 담관염 등을 유도한 다양한 동물 모델에서 LAPSTriple Agonist의 지방간과 간염증, 특히 간 섬유화(fibrosis)에 대한 뛰어난 효능을 확인한 연구 결과를 구연 발표한다.
한미약품은 해당 연구를 통해 경쟁약물인 FXR agonist(성분명: 오베티콜산) 대비 다양한 섬유화 마커 및 조직학적 간 섬유화 개선 효과를 확인했다. LAPSTriple Agonist는 지난 3월 미국 FDA에 의해 원발 담즙성 담관염 및 원발 경화성 담관염 치료를 위한 희귀의약품으로 지정된 바 있다.
한미약품 대표이사 권세창 사장은 "현재까지 획기적 치료제가 없는 NASH 분야에서 한미의 랩스커버리 기반 여러 바이오신약들이 세계에서 가장 우수한 신약으로 개발될 수 있을 것으로 본다"며 "도전과 혁신을 통해 글로벌 신약개발에 매진하겠다”고 말했다.
LAPSTriple Agonist에 적용된 한미의 독자 플랫폼 기술 ‘랩스커버리’는 다양한 영역의 혁신신약으로 확장되고 있다. 30여개에 이르는 한미약품의 신약 파이프라인 중 최근 MSD에 기술수출된 LAPSGLP/GCG(듀얼아고니스트)와 미국 FDA에서 시판허가를 심사중인 롤론티스(Rolontis) 등 13개 파이프라인에 랩스커버리 기술이 적용됐다.
















