기업
이태훈 전남대 교수팀, “골질환 치료 저분자 물질 발굴”
바이오스펙테이터 서일 기자
[바이오파마테크콘서트] 이태훈 전남대 교수 연구팀, 파골세포 분화 억제성 저분자 물질 선별.. “골다공증”등 골질환 치료 후보물질 기대

이태훈 전남대 교수 연구팀은 골질환의 원인이 되는 과다한 파골세포의 분화를 억제할 수 있는 저분자 물질을 발굴했으며, 추가 연구를 통해 선도물질 및 후보물질을 선정할 것이라고 밝혔다.
이 교수는 지난 16일 개최된 제 11회 바이오파마테크콘서트에서 ‘골질환 예방 또는 치료용 약학 조성물’이라는 주제로 골 흡수를 억제하는 저분자 조성물과 선별한 물질의 파골세포(Osteoclast) 분화 억제효능에 대해 발표했다.
이 교수는 “손상된 뼈가 제거되어 재흡수되는 과정은 정상적인 재생과정이지만, 재흡수가 심해짐에 따라 골다공증, 만성 치주염, 류마티즘, 건선성 관절염과 같은 질병이 발생한다”며 “이러한 골질환들은 뼈의 재흡수와 관련된 파골세포의 분화를 조절함으로써 질환 개선의 가능성이 있다”고 말했다.
뼈의 재생은 골을 흡수하는 파골세포와 골을 생성하는 조골세포(Osteoblast)에 의해 작동한다. 파골세포는 대식세포(Macrophage)로부터 M-CSF(Macrophage-colony stimulating factor)와 RANKL(Receptor activator of nuclear factor-κB ligand)이라는 특정 리간드의 신호전달 체계에 의해 분화된다. 파골세포의 분화가 과다하게 일어날 경우 골다공증과 같은 골질환을 유발하기 때문에, 파골세포의 분화를 조절하는 방향으로 이러한 골질환의 치료제가 개발된다. 이 교수는 M-CSP, RANKL 등이 관여하는 신호전달 경로를 막는다면, 과다한 파골세포의 분화를 억제할 수 있다고 설명했다.
이교수 연구팀은 파골세포 분화를 유도하는 신호전달체계 단백질에 대한 저분자 물질을 발굴했다. In vitro 상에서 BMM(Bone marrow derived macrophage)을 파골세포로 분화시켜, 이 과정에서 발현되는 단백질에 대한 동정을 실시했다. 동정한 단백질과 상호작용하는 저분자 물질 중 최종적으로 #25, #35, #13, #45와 각각의 저분자 물질에 대한 유도체들을 선별하였고 이들의 파골세포 분화 억제능을 실험했다.
선별한 4종류의 저분자 물질들은 모두 파골세포의 분화를 확실히 억제했지만, 각기 다른 신호 전달 단백질에 관여하는 것으로 나타났다. 예를 들어, #25 물질은 RANKL이 RANK(Receptor)에 붙는 과정을 억제하며, #25의 유도체인 #25-D5, D7의 경우 NFATc1이라는 전사인자를 억제하여 파골세포 분화에 관여하는 유전자 활성을 억제한다. #13 저분자 물질은 직접적인 파골세포의 분화 신호 체계는 아니지만, 프롤린 이성질화효소(Prolyl isomerase)의 안정화를 유도함으로써 파골세포의 분화를 저해하는 것으로 나타났다.
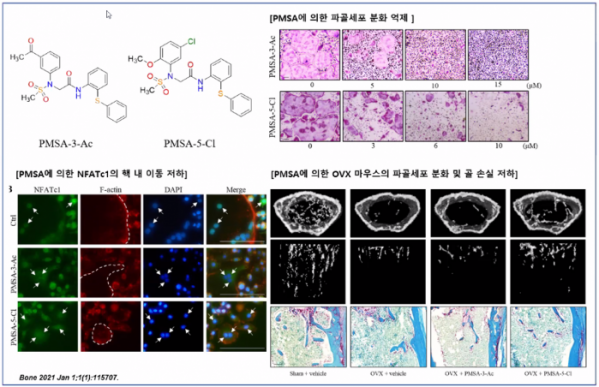
▲선별한 #25 저분자 물질의 파골세포 분화 억제 결과(이태훈 교수 연구팀 발표자료 캡쳐)
현재 이 교수 연구팀은 발굴한 저분자 물질에 대한 유효물질 연구단계(HIT) 중에 있으며 앞으로 선도물질(Lead) 및 후보물질(Candidate) 연구와 비임상 실험을 진행할 계획이라고 덧붙였다. 이 교수 연구팀은 선별한 저분자 물질에 대해 7건의 국내 특허와 2건의 PCT 국제 특허를 출원했다.













![[인사]대원제약, 2026년 정기 승진 인사](https://img.etoday.co.kr/crop/77/77/1956956.jpg)




