오피니언
리듬, 유전성 비만 2상 “'MC4R' 넓은 변이까지 효능"
바이오스펙테이터 노신영 기자
POMC, PCSK1 및 LEPR 유전자 결함, SRC1, SH2B1 결핍 비만 환자 대상 체중 감소 효과, 소아 BBS 환자 대상 BMI-Z score 감소 확인.. 자체 유전자 DB 활용한 MC4R 관련 신규 31개 유전자 대상으로 적응증 확대 임상 계획

리듬 파마슈티컬스(Rhythm Pharmaceuticals)가 유전성 비만질환 치료제 ‘임시브리(IMCIVREE™, Setmelanotide)’의 적응증 확대를 위한 POC(Proof-of-concept) 임상 결과를 발표했다. 리듬은 임상 결과와 함께, 앞으로 진행할 유전자 큐레이션(Gene curation) 기반의 중개연구(Translational Research) 계획을 발표했으며 이를 토대로 임시브리의 적응증 확대가 이뤄질 전망이다.
리듬은 지난달 26일(현지시간) MC4R(Melanocortin-4 receptor) 관련 유전자 결함 비만 환자를 대상으로 진행한 세트멜라노타이드(Setmelanotide) 평가 바스켓(basket, 특정 치료법에 대한 다중 질환 대상 임상) 임상 2상 결과를 발표했다. 세트멜라노타이드는 임시브리의 성분명으로, 지난 2020년 11월 미국 식품의약국(FDA)승인을 받은 유전성 비만 치료제다.
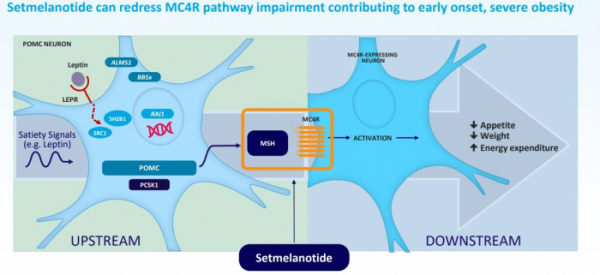
기존의 세트멜라노타이드가 POMC, PCSK1, LEPR 결핍이 있는 환자에게 처방하는 치료제라면, 이번 발표에서 리듬은 두쌍의 유전자 가운데 하나에만 변이를 가진 이형접합(Heterozygous) 환자와 새로운 유전자 변이인 SRC1, SH2B1 결핍 비만 환자까지 약물 효능이 있다고 발표했다. 리듬은 해당 유전자 변이까지 포함한다면 세트멜라노타이드를 적용할 수 있는 환자 수가 약 6만7000명으로 증가한다고 예측했다. 아직 임상 결과를 발표하지 않은 추가적인 적응증까지 포함한다면 약 8만명의 잠재적인 환자가 세트멜라노타이드의 적용 대상이 될 수 있다고 설명했다.