기업
의약품 생산ㆍ영업 위탁 급증, '복제약 돈버는 시대' 저무나
바이오스펙테이터 천승현 기자
작년 생동성승인 복제약 중 80% 위탁..허가요건완화ㆍ영업대행 활성화로 시장 재편
국내 시장에서 신규 허가를 받은 복제약(제네릭) 제품 5개 중 4개는 직접 생산하지 않고 다른 업체에 위탁 생산하는 것으로 나타났다. 제약사들의 제조시설 확대와 위탁 의약품 허가 요건 완화로 인해 위수탁 시장이 확대될 전망이다. 제네릭 제품의 범람으로 제네릭 전문 업체와 연구개발(R&D) 중심 업체로 시장 판도도 재편될 것이란 예상도 나온다.
◇위탁 제네릭 급증..작년 직접 생산 제네릭보다 4배↑
22일 식품의약품안전처에 따르면 지난해 생물학적동등성(생동성) 인정품목은 총 1215개로 집계됐다. 생동성 인정품목은 식약처로부터 오리지널 의약품과 생동성시험을 통해 동등성을 인정받은 제품을 말한다. 지난해 1215개의 제네릭이 식약처 승인을 받았다는 의미다.
생동성 인정품목은 2012년 588개 품목에서 지속적으로 상승세를 나타내다 3년 만에 2배 이상 뛰었다. 지난 2004년 1648개 품목으로 정점을 찍은 이후 12년 만에 가장 많은 제네릭 제품이 지난해 쏟아졌다.
특히 직접 생동성시험을 진행한 제네릭보다 다른 업체에 생산을 의뢰하는 위탁 허가가 압도적으로 많았다는 점이 눈에 띄는 변화다. 지난해 생동성을 인정받은 1215개 품목 중 직접 생동성시험을 실시한 제품은 238개로 집계됐다. 위탁 제네릭은 977개로 전체의 80.4%를 차지했다.
위탁 제네릭은 다른 업체에 생산을 맡기는 제네릭 제품으로 수탁업체가 진행한 생동성시험 자료로 허가를 받는다. 지난해 승인받은 제네릭 중 제약사가 직접 생산하는 제품은 5개 중 1개에 불과하다는 얘기다.
위탁 제네릭은 지난 2004년(1291개) 이후 감소 흐름을 나타내다 2011년부터 증가하기 시작했다. 지난 2010년 위탁 제네릭은 190개에서 지난해 977개로 5년 만에 5배 이상 늘었다. 지난 2012년 위탁 제네릭이 자체 생산 제네릭 개수를 넘어선 이후 격차는 점차 벌어지고 있다.
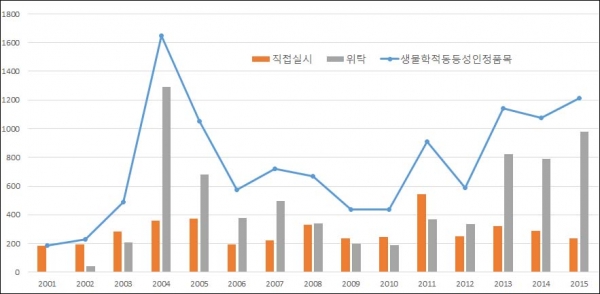
▲연도별 생물학적동등성인정품목 현황(단위: 개, 자료: 식품의약품안전처)
업계에서는 현재 유통되는 제네릭 품목 수만 따지면 위탁 제네릭이 직접 생산 제네릭보다 월등히 많을 것으로 추산한다. 제약사들이 위탁 제품과 직접 생산실적 제품의 생산실적을 구분해서 보고하지 않아 정확한 위탁 의약품 시장 규모는 파악되지는 않지만 제네릭 시장에서는 위탁 제품의 생산량이 전체의 20%를 웃돌 것으로 추정한다.
제약사들 공장 신증축ㆍ허가제도 변화로 위수탁 시장 팽창
국내 의약품 시장의 환경과 제도 변화에 따른 현상으로 분석된다.
업계 한 관계자는 “2000년대 들어 제약사들이 공장 신증축을 통해 대규모 생산시설을 확보하면서 남는 생산시설 활용을 위해 수탁 시장에 집중적으로 뛰어들었다”고 전했다.
지난 2012년 한국제약협회 조사를 보면 녹십자, 유한양행, JW중외제약, 한독, 대한약품, 안국약품, 휴온스 등 35개사가 수탁을 희망하는 것으로 나타났다. 업계에서는 현재 50곳 이상이 수탁 사업을 진행하는 것으로 파악된다.
이미 세파 계열 항생제나 항암제의 경우 별도로 분리된 제조시설에서만 생산이 가능해 한미약품, 일동제약, 경보제약 등 공장을 갖춘 업체를 중심으로 위수탁 시장이 활성화된 상태다. 여기에 최근 신증축한 공장의 가동률을 높이기 위해 수탁 영업도 치열하게 전개되는 추세다.
셀트리온제약이 지난해 3월 충북 오창에 1500억원을 들여 국내 최대 규모의 합성의약품 공장을 준공한 것도 수탁 시장을 염두에 둔 것으로 보인다. 셀트리온제약이 지난해부터 허가받은 제네릭은 무려 72개에 달한다.
대웅제약은 주력제품 ‘알비스’의 제네릭을 직접 생산해 제약사 20여곳에 공급하는 방식으로 수탁 사업을 진행한다. 최근에는 한국콜마, 대원제약 등이 적극적으로 수탁 사업을 전개 중이다.
정부도 특정 제품의 집중 생산을 통한 품질개선을 유도하기 위해 제약사들의 위수탁을 적극 장려하는 분위기다.
위탁 제네릭의 시장 진입 장벽도 크게 낮아졌다. 지난 2011년 11월 공동 생동 규제가 폐지된 이후 위탁 제네릭 증가세가 가팔라졌다.
당초 식약처는 같은 공장에서 생산한 제네릭이더라도 생동성시험은 2개사까지만 함께 진행토록 제한하는 공동(위탁)생동 제한 규정을 시행했다.
같은 공장에서 똑같은 공정을 통해 같은 성분의 6개 제네릭을 생산하더라도 생동성시험은 2개씩 3그룹으로 나눠서 진행해야 한다는 의미다. A제약사가 B사가 생산중인 제품을 제품명만 다르게 위탁받아 생산하고 허가를 받을 때에도 A사가 별도로 생동시험을 진행해야만 허가를 내줬다. ‘같은 공장에서 생산하는 똑같은 의약품인데도 임상시험을 따로 진행하토록 하는 것은 불합리한 규제’라는 제약업계의 지적에 2011년 이 규제는 사라졌다.
위탁 제네릭 진입 장벽 완화는 여기에 그치지 않는다. 지난 2014년 의약품을 생산하는 모든 공장은 3년마다 식약처가 정한 시설기준을 통과해야 의약품 생산을 허용하는 내용의 ‘GMP 적합판정서 도입’이라는 새로운 허가 제도를 시행하면서 허가용 의약품을 의무적으로 생산해야 하는 규정이 큰 폭으로 완화됐다.
기존에는 다른 업체가 대신 생산해주는 위탁 의약품이 허가를 받으려면 3개 제조단위(3배치)를 미리 생산해야 했지만 적합판정을 통과한 제조시설에서 생산 중인 제네릭을 제품명과 포장만 바꿔 허가받을 때 절차가 간소화됐다.
이에 따라 제약사 입장에서는 허가 신청 수수료 92만원 가량만 부담하면 별도의 생동성시험과 허가용 의약품 생산 절차를 거치지 않고도 위탁 제네릭 허가가 가능해졌다.
또 2012년 약가제도 개편으로 시장에 늦게 진입하는 제네릭도 최고가를 받을 수 있어 후발주자들의 제네릭 시장이 크게 늘었다. 한국제약협회에 따르면 올해 1월 1일 기준 제네릭 개수가 50개 이상 등재된 성분은 63개에 달한다. 현재 오리지널 의약품 63개 시장에 최소 3150개의 제네릭이 경쟁한다는 의미다. 4년 전에는 제네릭이 50개 이상 등재된 시장은 20개에 그쳤다.
영업환경 변화도 제네릭 개수 증가에 기여한다는 분석도 제기된다. 최근 전문 영업 대행 업체(CSO, Contract Sales Organization)를 활용한 제네릭 영업도 활성화되고 있다.
CSO는 제약사가 일정 비용을 지불하고 특정 제품의 영업을 전담하는 업체다. 주로 제약사 영업사원 출신으로 구성됐다. 신흥 업체나 영세 제약사를 중심으로 자체 영업조직을 구축하지 않고 CSO를 활용한 제네릭 영업이 늘고 있다는 뜻이다.
업계 한 관계자는 “몇 년 전만 해도 수탁 경쟁의 과열로 수탁 가격을 지나치게 떨어뜨려 시장을 교란하는 사례도 빈번했지만 최근에는 위탁 수요가 급증하면서 수탁 업체의 위상이 높아지고 있다”고 말했다.
◇"제네릭 시장으로 돈 버는 시대 종료"..시장판도 재편 예고
업계 일각에서는 제네릭 난립을 차단하기 위해 시장 진입 장벽을 높여야 한다는 지적도 제기하지만 뽀족한 방법을 찾기는 힘든 실정이다.
최근 식약처가 허가 수수료 상향 조정으로 제네릭 허가 수수료가 약 92만원에서 139만원(제조시설 평가를 받지 않을 경우)으로 종전보다 50% 가량 상승했지만 제약사 입장에선 큰 부담이 되는 수준은 아니다.
오히려 국내 의약품 시장 판도가 신약과 제네릭 업체로 양분될 것이란 분석도 나온다. 제네릭 사업으로 큰 수익을 내기 힘들다는 이유에서다. 실제로 최근에는 삼진제약의 '플래리스', 종근당의 '리피로우'와 같은 대형 제네릭의 출현을 찾기 어렵다.
업계 한 관계자는 “최근 제네릭 제품들이 봇물처럼 쏟아지면서 제네릭으로 돈을 벌기는 힘들어졌다”면서 “향후에는 신약과 개량신약으로 승부하는 업체와 제네릭만을 집중적으로 뛰어드는 업체로 구분되는 형식의 시장 재편 가능성이 높다”고 분석했다.



















