기업
삼성 RA시밀러 3총사, '항-약물 항체' 발생률 살펴보니..
바이오스펙테이터 장종원 기자
EULAR에서 임상 ADA∙방사선상 변화 분석 결과 발표.."ADA도 오리지널과 유사"
삼성바이오에피스 류마티스 관절염 바이오시밀러 3총사의 항-약물 항체 발생률이 오리지널의약품과 유사한 것으로 나타났다. 바이오시밀러의 효능, 안전성뿐 아니라 항-약물 항체 발생률까지 오리지널 바이오의약품과 유사함을 확인한 것이다. 항-약물 항체(Anti-Drug Antibodies; ADA)는 면역원성에 의해 발생하는 약물에 대한 항체로 TNF-α 억제제의 효과를 저해하는 요인이다.
삼성바이오에피스는 13일(현지시간) 네덜란드 암스테르담에서 개최된 유럽 류마티스 학회(EULAR))에서 베네팔리(성분명 에타너셉트), 플릭사비(성분명 인플릭시맙), 임랄디(성분명: 아달리무맙) 3종의 TNF-α 억제제 바이오시밀러의 임상 분석 결과를 발표했다. 오리지널의약품과 효능과 안전성을 비교한 기존의 임상3상 데이터에 항-약물 항체(ADA)와 방사선상의 변화를 분석한 데이터를 통합한 것이다.
삼성바이오에피스는 3종의 바이오시밀러 임상 3상에 참여한 대상자 1710명을 대상으로 약효 및 질병의 진행활성과 ADA의 관련성 등을 분석했다.

비교 분석 결과, ADA가 발생한 환자보다 ADA가 발생하지 않은 환자가 더 큰 효능을 본 것을 확인했다. 증상이 20% 이상 경감된 것을 의미하는 지표인 ‘ACR20’ 반응률이 ADA가 발생하지 않은 환자가 더 높게 나타났다. 28개 관절의 질환 활성을 평가하는 ‘DAS28’ 지표에서도 ADA가 발생하지 않은 환자가 더 좋은 호전양상을 보였다. 이는 ADA 발생과 환자의 치료효과 간의 상관관계를 짐작할 수 있게 해준다.
ADA가 발생한 환자의 비율은 오리지널의약품과 바이오시밀러가 유사하게 나타났다. 인플릭시맙은 ADA 발생률이 플릭사비는 55.1%, 레미케이드는 49.7%로 나타났고 아달리무맙은 임랄디 33.1%, 휴미라 32%로 유사했다. 반면 에타너셉트의 경우 베네팔리의 ADA 발생률은 0.7%로 엔브렐(13.1%)보다 크게 낮았다.
삼성바이오에피스는 방사선상의 변화 분석 결과도 내놨다. 이들은 바이오시밀러 임상3상에 참여한 1263명 환자의 방사선 사진 데이터를 수집해 평가시점(24주/30주)에서 DAS28 지표에 따라 관해(remission)군, 저활성(LDA)군, 중활성(MDA)군, 고활성(HDA)군으로 그룹화했다. 방사선적 진행에 대한 평가는 0주와 52주 또는 54주 시점에서 관절염 진행억제 효과를 평가하는 mTSS(modified Total Sharp Score; 점수가 높을수록 나쁨) 지표 변화와 방사선적 자료에서 병기가 진행되지 않은 것으로 관찰되는 환자의 수를 기준으로 진행됐다.
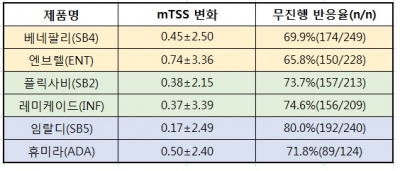
평가 결과, 모든 그룹에서 방사선상 변화 발생이 줄어들었으며, 바이오시밀러를 적용한 그룹이 오리지널의약품 적용군보다 변화가 낮은 경향을 보였다. 또한 병기가 진행되지 않은 것으로 관찰된 환자를 비교했을 때에도 오리지널의약품 대비 더 높은 비율로 관찰됐다.
삼성바이오에피스는 이외에도 ‘베네팔리와 오리지널의약품 간 치료효과 비교 연구’ 등 6개의 Real World Data가 이번 학회에서 공개됐다.
한편, 삼성바이오에피스가 개발한 엔브렐 바이오시밀러 베네팔리와 레미케이드 바이오시밀러인 플렉사비는 2016년부터 유럽 23개 국가에서 판매됐으며 약 8만명의 환자에게 처방됐다. 휴미라 바이오시밀러인 임랄디는 지난해 8월, 유럽에서 판매 허가를 승인받고 올해 10월부터 유럽에서 판매가 진행될 예정이다.


















