국제
웨이브, 엑손 스키핑 치료제 '수보더센' 1상 결과발표
바이오스펙테이터 서일 기자
카이랄리티 고정해 효율높인 엑손 스키핑(Exon skipping) 치료제 ‘수보더센’..FDA, 임상 2/3상 CID 선정

싱가포르 웨이브 라이프 사이언스(Wave life sciences)는 미국 플로리다에서 열린 ‘2019 MDA Clinical and Scientific Conference’에서 뒤센 근이영양증(Duchenn muscular dystrophy) 환자를 대상으로 진행한 엑손 스키핑(Exon skipping) 치료제 ‘수보더센(Suvodirsen, WWE-210201)’의 임상 1상(NCT03508947) 결과를 지난 16일(현지 시간) 발표했다.
뒤센 근이영양증은 디스트로핀(Dystrophin) 유전자의 엑손 49, 50이 결실되어 발병한다. 엑손 49, 50이 제거되면서 중지 코돈(Stop codon)이 생기는데, 단백질 합성이 중단되어 기능하지 못하는 디스트로핀이 만들어진다. 디스트로핀은 근 세포막(Sarcolemma)에 있는 세포골격(Cytoskeleton) 단백질이다. 뒤센 근이영양증 환자는 근육의 발달이 저하된다. 심장근, 호흡근에도 영향을 미쳐 20세 이전에 사망한다. 유병률은 10만 명당 약 4명이며, 남자아이의 경우 3500명당 1명 정도 발생하는 것으로 알려졌다.
85일간 진행된 임상 1상은 뒤센 근이영양증 환자 36명을 대상으로 ‘수보더센’을 주 1회 정맥 주사로 투여했다. 용량은 0.5mg/kg, 1mg/kg, 2mg/kg, 5mg/kg, 7mg/kg(또는 10mg/kg) 5가지로 나누어 진행됐으며, 치료제의 안전성, 내약성을 평가했다.
‘수보더센’ 투여그룹 67%, 위약그룹 80%에서 발열, 두통, 구토, 빈맥이 확인됐지만, 중등도의 부작용은 없었다. 다만 고용량인 5mg/kg, 7mg/kg(또는 10mg/kg) 투여그룹에선 hsCRP(high sensitivity C-Reactive Protein), 보체 인자 Bb(Complement factor Bb) 수치가 증가한 것이 확인됐다. 증가한 수치 모두 1주일 이내에 해결됐으며, 이상 반응을 보인 환자의 보체 C3 변화는 없었다.
현재 출시된 엑손 스키핑 치료제 중 뒤센 근이영양증 환자를 대상으로 사용하는 것은 ‘에테플러센(Eteplirsen)’이다. 사렙타 테라퓨틱스(Sarepta Therapeutics)가 개발한 ‘에테플러센’은 엑손 51을 표적으로 작용한다. ‘에테플러센’은 PMO ASO(Phosphorodiamidate Morpholino Antisense Oligonucleotide)다. 디스트로핀 유전자의 pre-mRNA에 안티센스(Antisense)로 결합하여 엑손 51이 발현되지 않도록 억제한다. 엑손 51이 억제되면 길이는 짧아도 기능할 수 있는 디스트로핀이 만들어진다. ‘에테플러센’은 pre-mRNA와 시퀀스(Sequence)가 일치해야 작용할 수 있기에, 전체 뒤센 근이양증 환자 중 1%에서만 치료 효과가 있는 것으로 추정된다.
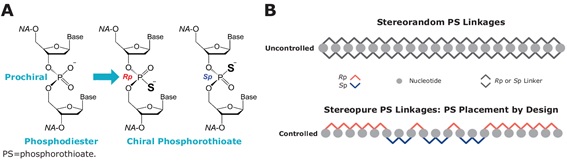
▲웨이브 라이프 사이언스 2018 OTS 발표자료(Figure 2).
‘수보더센’도 안티센스로 결합하여 디스트로핀 유전자의 엑손 51 발현을 억제한다. 다른 점이 있다면 PS(Phosphorothioate)로 올리고머의 카이랄리티(Chirality)를 고정했다.
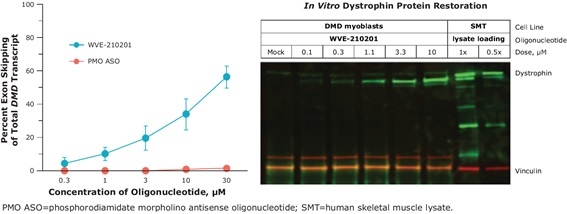
▲웨이브 라이프 사이언스 2018 OTS 발표자료(Figure 3).
웨이브 라이프 사이언스는 비 임상 시험에서 ‘수보더센’의 엑손 스키핑 효율이 PMO ASO보다 높은 것으로 확인했으며, ‘수보더센’은 뒤센 근이양증 환자 중 13%에게 치료 효과가 있을 것으로 예상한다.
웨이브 라이프 사이언스는 비 임상 시험, 임상 1상 자료를 토대로 임상 2/3상(DYSTANCE 51, NCT03907072)에서 사용할 ‘수보더센’ 용량을 결정했다. 48주간 참여하는 150명의 환자에게 4.5mg/kg 또는 3mg/kg을 주 1회 정맥 주사로 투여하여 위약 그룹과 비교할 계획이다. 1차 종결점은 디스트로핀 단백질 농도의 변화와 NASS(North Star Ambulatory Assessment)에서 정한 뒤센 근이영양증 진단기준으로 설정됐다. 2차 종결점은 근력, 달리기 등 근육의 기능을 측정하는 것으로 설정됐다. ‘수보더센’ 임상 2/3상은 미국 FDA로부터 CID(Complex Innovative trial Design) 프로그램으로 선정됐으며, 오는 7월 시작될 예정이다.


















