국제
‘GSK-3β 억제제’ 액츄에이트, 2170만弗 시리즈B 유치
바이오스펙테이터 서일 기자
치료 저항성 암세포의 새로운 치료 표적 물질 ‘GSK-3β’..GSK-3β 억제제 ‘9-ING-41’ 전임상에서 교모세포종 완전한 퇴화 확인

GSK-3β(Glycogen Synthase Kinase-3β) 억제제이자 저분자 화합물 '9-ING-41'를 개발하고 있는 미국 액츄에이트 테라퓨틱스(Actuate Therapeutics)가 2170만달러의 시리즈B를 유치했다고 지난 14일(현지 시간) 발표했다. 액츄에이트는 이번 시리즈B로 9-ING-41 임상 1/2상(1801, NCT03678883) 진행에 필요한 자금을 확보했다.
이번 시리즈B 투자에는 카이로스 벤쳐스(Kairos Ventures), 바이오스 파트너스(Bios Partners), 데프타 파트너스(DEFTA Partners), 테크 코스트 앤젤스(Tech Coast Angels)가 참여했다.
다니엘 슈미트(Daniel Schmitt) 액츄에이트 CEO는 “이번 자금확보로 미국에서 진행하는 1801 연구에 속도를 낼 수 있게 됐다”며 “유럽의 암 연구 협회와 협력해 유럽에서도 1801 연구를 진행할 수 있게 됐다”고 밝혔다.
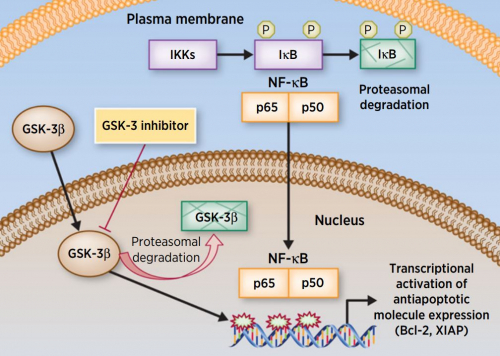
▲GSK-3β 억제제 작용기전(DOI: 10.1158/1078-0432.CCR-15-2240)
GSK-3β는 알츠하이머, 양극성 장애, 제2형 당뇨병 등의 질환이 유발된 세포에서 섬유화를 촉진한다. 특히, 화학요법, 방사선요법에 치료 저항성을 가진 악성 암세포의 핵에 다량 축적된 것이 발견됐다. GSK-3β는 NF-κB 신호 경로를 촉진해 암세포의 치료 저항성 획득, 증식에 관여하는 것으로 알려졌다. 액츄에이트는 GSK-3β를 억제하면 항암 효능을 보일 수 있을 것으로 내다봤다.
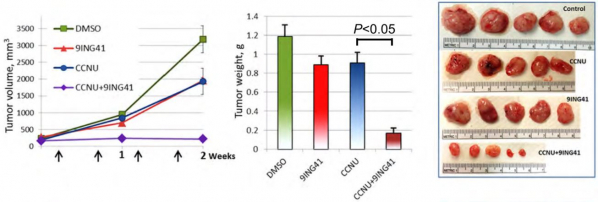
▲9-ING-41 전임상시험 결과(DOI: 10.1016/j.tranon.2017.06.003)
액츄에이트는 동물실험모델 대상 9-ING-41, 뇌종양 치료제 로무스틴(CCNU, Lomustine) 병용 전임상연구에서 교모세포종의 증식을 억제하는 것에 성공했다. 화학요법 저항성을 가진 교모세포종 환자의 암세포를 쥐에 이식한 실험모델에서 9-ING-41은 CCNU과 유사한 수준의 교모세포종 증식 억제를 보였다. 9-ING-41, CCNU 병용한 경우 종양 증식은 더 큰 수준으로 억제됐다.
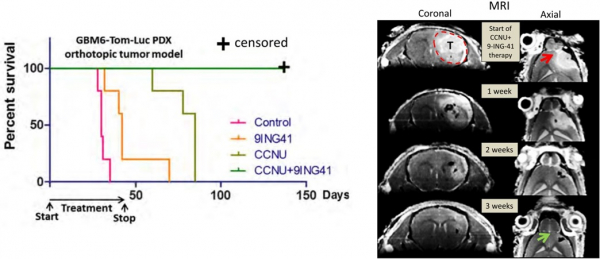
▲9-ING-41 전임상시험 결과(DOI: 10.1016/j.tranon.2017.06.003)
9-ING-41, CCNU 병용은 교모세포종을 이식받은 실험모델의 생존율을 100%로 끌어올렸으며, MRI에서 3주만에 완전한 종양 퇴화를 보였다.
미국 식품의약국(FDA)은 지난 2017년 8월 9-ING-41을 희귀의약품(Orphan Drug)으로 지정했다.
현재 액츄에이트는 림프종, 췌장암, 교모세포종 등 치료 저항성을 가진 암 환자를 대상으로 1801 연구에 참여할 환자를 모집하고 있다.














