기업
바이오파마 테크콘서트 공개 5가지 신약물질은?
바이오스펙테이터 장종원 기자
20일 제약바이오協서 기술소개 및 파트너링 진행..항균 펩타이드·오토파지 NASH/알츠하이머병 치료제·TLR 제어 신약·저분자 화합물 기반 세포치료제 개발 플랫폼 소개
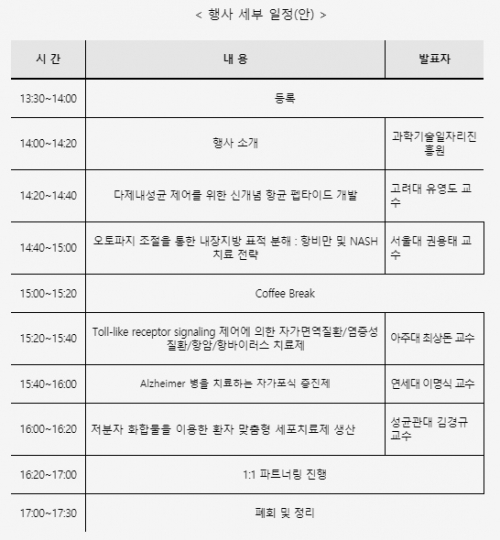
오는 20일 서울 방배동 한국제약바이오협회에서 개최되는 '2019년 제1회 바이오파마 테크콘서트'에서는 총 5가지 기술이전·사업화 가능 기술이 소개된다.
▲다제내성균 제어를 위한 신개념 항균 펩타이드 개발(유영도 고려대 교수), ▲오토파지 조절을 통한 내장지방 표적 분해 : 항비만 및 NASH 치료 전략(권용태 서울대 교수), ▲Toll-like receptor(TLR) signaling 제어에 의한 자가면역질환, 염증성질환, 항암, 항바이러스 치료제(최상돈 아주대 교수), ▲알츠하이머병을 치료하는 자가포식 증진제(이명식 연세대 교수), ▲저분자 화합물을 이용한 환자 맞춤형 세포치료제 생산기술(김경규 성균관대 교수)이다.
이번 행사의 공동주관사인 바이오스펙테이터는 테크콘서트에 앞서 이들 기술을 간략히 소개한다. 이번 행사에 참석하면 해당 연구자의 자세한 기술 소개 및 파트너링이 가능하다. <참가 신청 : 성명/소속기관/직위/연락처(H.P, e-mail)/파트너링 요청기술(선택) 등 작성해 이메일(mhj9825@compa.re.kr)로 신청>
다만 유영도 고려대 교수의 '다제내성균 제어를 위한 신개념 항균 펩타이드'는 특허 출원 전이어서 행사 당일에 공개된다. 현재 전임상 진입을 위한 후보물질 완성 단계로 균혈증, 패혈증, 피부 감염 질환, 요로 감염증 등에 적용 가능하다는게 유 교수의 설명이다.
①라포파지 조절 통해 내장지방 표적분해
권용태 서울대 교수는 '오토파지 조절을 통한 내장지방 표적 분해 : 항비만 및 NASH 치료 전략'을 발표한다. 오토파지의 일종인 리포파지 조절을 통해 내장지방을 표적 분해하는 기술이다. 중추신경계에 영향을 주지 않는 무독성 항비만치료제 개발이 가능한 기술이라는 설명이다.
권 교수는 비만 마우스모델에서 그 가능성을 봤다. 고지방 식이 비만 마우스 모델에서 8주 투여 후 내장지방이 4분의 1로 줄어들었으며 체중은 대조군 대비 22% 감량됨을 확인했다. 또한 대조군이 지방간으로 발전하는데 반해, 리포파지 조절제를 투여한 마우스 간은 정상을 유지했다.
권 교수는 "간에 축적된 지방은 지방 독성을 유발해 염증 및 섬유화를 유발한다. 지방 과립의 제거는 염증을 완화하고 임상적 증상을 호전시킬 수 있을 것"이라면서 "실제 비만 마우스 모델에서 간의 염증 세포인 마크로파아지(macrophage)가 감소됐다"고 설명했다.
이 기술은 고도비만, 비만형 당뇨, 지방간, NASH, 간경화 등 신약부터 건강보조제 동물약 등으로 활용 가능하다.
②TLR 제어하는 저분자화합물·펩타이드 발굴
최상돈 아주대 교수는 'Toll-like receptor signaling' 제어에 의한 자가면역질환, 염증성질환, 항암, 항바이러스 치료제를 소개한다. 최 교수는 Toll-like receptor signaling 주변 타깃분자 제어용 저분자화합물 또는 펩타이드를 발굴했다.
먼저 TNFα(Tumor necrosis factor α) 억제제인 TIM1은 200uM까지 인비트로 무독성을 관찰했다. TIM1은 현재 류마티스관절염 마우스를 이용한 효능입증 실험이 진행되고 있다.
또한 TLR 3/7/8/9 억제 기능이 있는 길항성 소분자 화합물 TAC5는 TNFα의 분비, NFkB 활성화, IkB 분해, MAPKs의 인산화를 차단할 뿐만 아니라 염증성 사이토카인의 생성을 억제함으로써 전신홍반루푸스, 건선 등을 비롯한 자가면역질환과 염증성질환의 예방 또는 치료용도로 가능성을 확인했다.
③알츠하이머병 표적 자가포식 증진제
이명식 연세대 교수는 '알츠하이머병을 치료하는 자가포식(오토파지) 증진제'를 소개한다. 최근 유전적 알츠하이머병 또는 보통의 비유전적 알츠하이머병 모두에서 자가포식의 저하 또는 자가포식 과정에서 단백질 분해를 실질적으로 수행하는 세포 소기관인 리소좀 기능의 저하가 중요한 기저 원인일 것이라는 증거가 전장유전체 연관 분석(GWAS) 연구 또는 환자의 조직을 이용한 연구에서 계속 나오고 있다.
이 교수는 대사 질환, 염증성 질환에 대해 효과가 있는 다수의 자가포식 증진제 화합물을 발굴했는데 이들 자가포식 증진제 화합물이 알츠하이머병에 효과가 있을 가능성이 있을 것이라는 가설 하에 연구를 수행했다.
그 결과 자가포식 증진제 화합물의 변형물(MSL-5)이 인비트로 연구에서 아밀로이드 단백질 및 타우 단백질 제거에 탁월한 효과가 있음을 관찰했다. 알츠하이머병 마우스 모델에서 행동 이상이 유의하게 호전됐으며 조직학적으로 두 단백질 축적이 현저히 감소했다. 알츠하이머병 발병에 중요한 역할을 하는 미세아교세포(microglia)의 염증 역시 유의하게 감소했다.
④저분자 화합물 이용한 세포치료제 개발 플랫폼
김경규 성균관대 교수는 환자의 체세포를 저분자 화합물을 통해 다른 세포로 전환하는 기술을 이용해 세포치료제를 개발하는 새로운 재생의학기술을 선보인다.
세포 재생이 어려운 난치성 및 퇴행성 질환의 치료를 위해서는 외부에서 생산된 세포의 이식을 통해 조직이나 장기의 기능을 회복시키는 세포 치료가 유용한 치료법으로 대두되고 있다. 현재 개발 중인 많은 세포치료제는 줄기세포를 기반으로 하고 있는데 이 경우 암 발생의 위험이 제기되고 있고 동종세포를 사용하는 경우 면역 거부반응의 문제를 해결해야 하는 단점이 있다는 설명이다.
김 교수는 저분자 화합물을 이용해 환자의 체세포(섬유아세포)를 세포치료제로 개발하는 플랫폼 기술을 확보했다. 그는 체세포로부터 전환된 세포 중 신경교세포의 활성을 지니는 세포를 신경손상 치료제로 개발 중이다. 마우스 모델을 통해 섬유아세포에서 전환된 유사신경교세포 (GLC)가 말초 및 중추신경재생효과를 갖는 것을 확인했다.














![[BioS 레터]무균주사제 공급망 변화와 CDMO 대응](https://img.etoday.co.kr/crop/77/77/2262816.jpg)



