국제
퍼진, '절제술 대신할' 방광암 유전자치료제 3상 '성공’
바이오스펙테이터 서일 기자
고위험도 비근육침습성 방광암 유전자치료제 인스틸라드린..방광절제술 대신 사용 가능..12개월 지속 완전관해 보이며 1차 종결점 충족..FDA 우선심사 진행 중

방광암 치료에서 방광절제술을 대신할 획기적인 치료제가 출시될 것으로 기대된다. 재발률이 높은 고위험도 비근육침습성 방광암과 치료가 어려운 유두종을 가진 방광암에 효과를 보인 유전자 치료제다. 미국 신약개발회사 퍼진(FerGene)은 고위험도 비근육침습성 방광암 유전자 치료제 인스틸라드린(INSTILADRIN®,nadofaragene firadenovec, rAd-IFN/Syn3)의 상업화 임상에서 1차 종결점을 충족시킨 결과를 내놨다.
이 치료제는 현재 미국 FDA에 바이오의약품 허가신청서(Biologic License Application, BLA)를 제출해 우선심사(Priority review)를 진행 중이다.
방광암 환자의 70% 이상은 비근육침습성 방광암(non-muscle invasive bladder cancer, NMIBC, CIS ± Ta/T1)으로 표준치료요법인 결핵 예방백신 BCG(Bacillus Calmette-Guérin)를 방광 내 주입해 치료해 왔다. 그러나 60% 이상이 재발하고 BCG에 반응을 보이지 않는 경우도 빈번했다. 이럴 경우 방광을 절제하는 치료를 할 수밖에 없어 환자 삶에 큰 영향을 주게 된다.
퍼진은 지난 6일(현지시간) 비뇨기과 종양학회(Society of urologic Oncology 20th Annual Meeting) 방광암세션(the bladder cancer session)에서 인스틸라드린을 투여받은 NMIBC 환자 53%가 3개월에 완전관해(complete response, CR)를 보이고 24% 환자가 12개월간 지속적인 완전관해를 보인 결과를 발표했다.
콜린 디니(Colin Dinney) MD앤더슨 암센터 비뇨기과장은 “현재 BCG 불응성 고위험도 NMIBC는 치료옵션이 거의 없고, 방광제거술은 예후가 좋지 않다”며 “ 방광제거술은 환자의 삶의 질과 직결된 수술이므로, 이번 임상 3상 결과는 매우 고무적이며 방광절제술을 해야 하는 환자들의 미충족의료수요를 해결해 줄 수 있을것이다”고 말했다.
인스틸라드린은 BCG 불응성 고위험도(high-grade) NMIBC에 대한 아데노바이러스 기반 유전자 치료제다. 인스틸라드린은 아데노바이러스 벡터에 인터페론-α2 유전자를 조합해 만들었으며, 암세포 주위의 세포에 들어가 인터페론-α2 단백질을 대량으로 분비하게 해 치료한다는 설명이다. 인터페론-α2는 세포증식억제와 면역반응을 활성화한다.
발표에 따르면 인스틸라드린은 치료가 어려운 환자군인 유두종(papillary disease)을 가진 방광암환자에게도 유효한 결과를 보였다. 미국에서 NMIB 환자 157명이 참여한 인스틸라드린 상업화 임상 3상에서 NMIBC 환자 53%는 3개월에 완전관해를 보였고, 24%는 12개월간 완전관해가 지속됐다. 추가적으로, 유두종을 동반한 NMIBC 환자 73%가 3개월간, 44%가 12개월간 무재발(high-grade recurrence-free, HGRF) 생존률을 보였다. 인스틸라드린은 3개월에 한번씩 환자의 방광에 주입됐다.
부작용도 거의 없었다. 가장 흔한 부작용은 피로, 오한, 열 등이었다. 4, 5등급 부작용은 보고되지 않았으며 1.9% 환자가 부작용으로 임상을 중단했다.
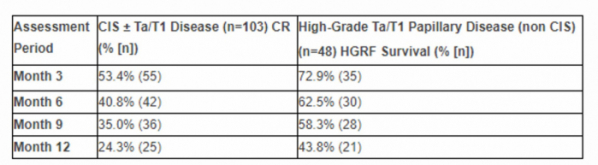
▲인스틸라드린 임상 결과(퍼링 파마슈티컬스 홈페이지 참조)
닐 쇼어(Neal Shore) 캐롤라이나 비뇨기과 연구센터 의료책임자는 "비뇨기과 전문의이자 임상 연구자로서, 혁신적인 치료옵션이 필요했던 고위험도 NMIBC 환자에게 이런 종류의 효능과 안전성을 보인 것이 고무적이다"며 “이 임상 결과는 NMIBC 환자에게 중요한 치료 옵션으로 인스틸라드린의 가치를 보여줄 것이다”고 말했다.
미국 제약회사 퍼진은 페링 파마슈티컬스(Ferring Pharmaceuticals)의 자회사로 블랙스톤 생명과학(Blackstone life science)과 페링이 공동투자해 만든 유전자 치료제 개발회사다. 페링에서 1억7000만달러, 블랙스톤에서 4억달러를 투자받아 미국내 인스틸라드린의 상업화 권리와 글로벌 임상개발을 위해 설립됐다. 페링은 스위스에 본사를 두고 있으며 소화기, 비뇨기 부분에서 전문성을 보이는 글로벌 바이오제약회사다.
유전자 치료제 인스틸라드린은 당초 핀란드 유전자치료제 전문개발회사 FKD 테라피스(FKD Therapies Oy)에서 개발됐으며, 지난 2018년 3월 페링으로 기술이전됐다.



















