국제
BMS, '옵디보+여보이' 중피종 1차 치료제 美FDA 승인
바이오스펙테이터 서일 기자
악성흉막중피종으로 적응증 확대..16년만의 FDA 승인 중피종 치료제
BMS(Bristol Myers Squibb)의 '옵디보(Opdivo, nivolumab)와 여보이(Yervoy, ipilimumab) 병용요법'이 악성흉막중피종 치료제로 미국 식품의약국(FDA)의 승인을 받았다. 이번 승인은 중피종 치료제에 대한 16년 만의 FDA승인이다.
BMS는 옵디보+여보이 병용요법이 수술로 종양을 제거할 수 없는 악성흉막중피종(Malignant Pleural Mesothelioma, MPM)에 대한 1차 치료제로 적응증을 확대해 지난 2일(현지시간) FDA의 승인을 받았다고 밝혔다. FDA는 중피종 치료제로 2004년 페메트렉시드(pemetrexed)+시스플라틴(cisplatin)병용요법을 승인한 바 있다. 그 후로 중피종 치료제에 대한 이번 FDA 승인이 처음이다.
옵디보와 여보이의 병용요법을 FDA 승인으로 이끈 임상 3상(NCT02899299)은 치료경험이 없고 수술로 종양을 제거할 수 없는 MPM 성인 환자를 대상으로 진행됐다. 임상은 옵디보+여보이 그룹(303명)과 기존의 화학요법 그룹(302명)으로 나누어 진행됐다. 옵디보+여보이 그룹의 환자들은 옵디보를 3주에 한번 360mg씩, 여보이를 6주에 한번 1mg/kg씩 투약했다. 옵디보+여보이 그룹의 전체생존기간(Overall Survivial, OS) 중간값은 18.1개월(95% CI: 16.8~21.5), 화학요법 그룹의 OS 중간값은 14.1개월(95% CI: 12.5~16.2)로 나타났다. 치료 2년째에 옵디보+여보이 그룹의 환자는 41%가 생존했고, 화학요법의 환자들은 27%가 생존했다.
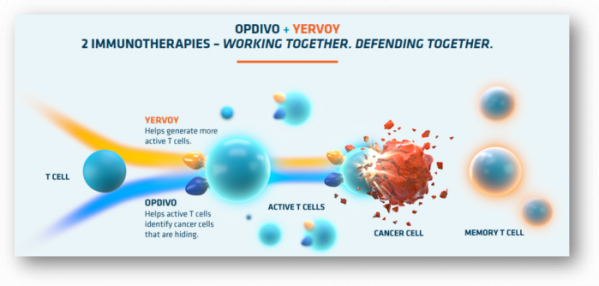
▲옵디보+여보이 작용 설명 그림(출처: 옵디보 홈페이지)
악성흉막중피종(Malignant Pleural Mesothelioma, MPM)은 석면 흡입이 주요한 원인이 되는 암이며, 미국에서 매년 2만명의 MPM 환자가 발생한다. MPM은 중피종에서 가장 흔하며, 대부분 늦게 발견되기 때문에 종양제거술을 할 수 없는 경우가 많다.
옵디보는 PD-1 receptor 항체로, 면역조절세포의 PD-1 receptor에 binding한다. 일부 암세포는 PD-1 receptor를 인지하여 면역반응이 일어나지 못하게 하는데, 옵디보는 이 과정을 막아 면역 시스템을 활성화시킨다. 여보이는 면역조절세포의 CTLA-4에 대한 항체다. 면역조절세포와 면역세포가 CTLA-4를 통해 상호작용하게 되면 면역세포의 활성은 저해된다. 여보이는 이 과정을 막아 면역세포를 활성화시킨다.
Richard Paxdur FDA 암연구센터 소장은 “이번 승인으로 MPM 환자의 전체생존기간의 향상을 증명한 옵디보+여보이 병용요법을 환자들에게 제공할 수 있게 되었다”며 “2004년에 승인한 페메트렉시드+시스플라틴 병용요법 이후 10년 넘는 시간이 지났고, 이제서야 중요한 다른 치료 옵션이 가능해졌다”고 말했다.




![[인사]일동제약, 신임 R&D 본부장에 박재홍 사장 선임](https://img.etoday.co.kr/crop/74/74/2316073.jpg)








![[인사]일동제약, 신임 R&D 본부장에 박재홍 사장 선임](https://img.etoday.co.kr/crop/77/77/2316073.jpg)




