오피니언
다인, 근육타깃 ASO "FDA 임상보류".."TfR 예의주시"
바이오스펙테이터 김성민 기자
FDA "추가 임상 및 비임상 데이터 요구"...앞서 일주일전 디날리의 BBB 투과 TREM2 항체도 美 임상보류 조치
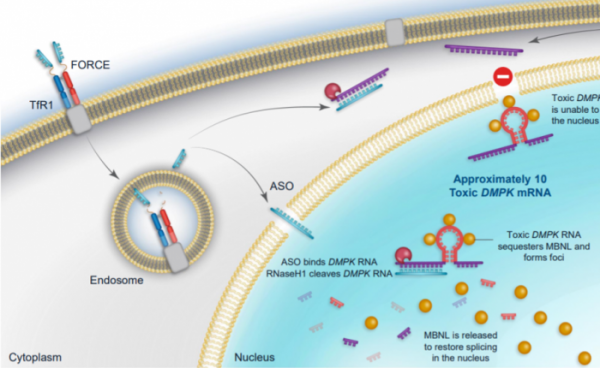
▲Dyne Therapeutics 플랫폼 소개자료
트랜스페린수용체(TfR) 기반 약물전달시스템을 적용한 신약 후보물질의 임상개발에 제동이 걸린 것일까? 1주일 사이 미국 식품의약국(FDA)이 2개의 TfR 약물전달시스템이 적용된 신약 후보물질에 대해 임상보류 조치를 내리면서, 업계는 잇따른 사건을 예의주시하기 시작했다. 각각 TfR을 기반으로 근육, 뇌를 타깃하는 약물이다. 아직 2개의 임상보류건 모두 구체적인 이유는 공개되지 않았다.
다인 테라퓨틱스(Dyne Therapeutics)는 미국 FDA으로부터 뒤센근이영양증(DMD) 후보물질 ‘DYNE-251’ 임상승인신청서(IND)에 대한 임상 보류통지를 받았다고 18일(현지시간) 밝혔다.
다인은 근육질환에 포커스해 TfR1 시스템을 매개로 근육조직으로 올리고뉴클레오타이드(oligonucleotide)를 전달하는 새로운 컨셉의 신약을 개발하는 회사다. 다인은 TfR1이 근골격근, 심장, 평활근(smooth muscle)에 높게 발현하고 있다는 것에 착안해, TfR1 수용체매개 전달시스템으로 약물전달 ‘FORCE’ 플랫폼을 구축하고 있는 회사다.
약물구조를 보면 TfR1 타깃 Fab(fragment antigen binding) 절편 1개에 링커로 올리고뉴클레오타이드 치료 효능을 발휘할 여러 페이로드(payload)를 결합시킨다. 다인은 표적에 따라 핵내 타깃은 ASO, 세포질 타깃은 siRNA를 부착한다. 다인은 크게 3가지 질환 ▲DMD ▲근긴장 디스트로피 타입1(DM1) ▲안면견갑상완형 근이영양증(FSHD) 등에 대한 포토폴리오를 구축하고 있다.... <계속>





![[인사]일동제약, 신임 R&D 본부장에 박재홍 사장 선임](https://img.etoday.co.kr/crop/74/74/2316073.jpg)







![[인사]일동제약, 신임 R&D 본부장에 박재홍 사장 선임](https://img.etoday.co.kr/crop/77/77/2316073.jpg)



![[인사]일동제약그룹, 2026년 정기 승진인사](https://img.etoday.co.kr/crop/74/74/2222747.jpg)

