국제
Summit, DMD 치료제 ‘Ezutromid’ 임상2상 실패
바이오스펙테이터 이은아 기자
1ㆍ2차 목표종결점 도달 실패.. '향후 C. difficile 항생제 개발 중점둘 것'

Summit Therapeutics가 개발한 듀센근이영양증(Duchenne muscular dystrophy, DMD) 신약후보물질 ‘Ezutromid’의 임상2상이 실패로 끝나면서 지난 27일 하루만에 주가는 78% 하락했다. 2016년 시작된 임상에서 1차 또는 2차 목표종결점을 만족시키지 못한 것이다.
DMD는 X염색체 상에 있는 디스트로핀(Dystrophin)의 유전자 변이로 디스트로핀 단백질 생성에 문제가 생겨 근육위축을 일으키는 유전성 희귀질환이다. Summit의 ‘Ezutromid’은 부족한 디스트로핀을 보완할 수 있는 유트로핀(utrophin) 단백질 수치를 높임으로써 DMD를 치료하도록 고안됐다. 유트로핀은 기능적, 구조적으로 디스트로핀과 유사한 자연발생 단백질로, 근섬유 발달 초기단계에서 생산되지만 성숙된 근육섬유에서는 발현되지 않는다. 이 때부터 디스트로핀이 생성되면서 동일한 역할을 수행한다.
임상2상은 디스트로핀이 부족한 5~10세의 남아 환자 40명을 대상으로 Ezutromid 1000mg 또는 2500mg 용량으로 하루 2회 경구 복용했다. 1차평가지수는 MRI를 통해 12, 24, 36, 48주째 다리근육 수치의 변화를 측정하고, 2차평가지수는 생검을 통해 유트로핀과 근육손실 정도를 평가하는 것이었다.
지난 1월, Summit은 임상2상의 24주째 중간결과 근육손실이 유의하게 감소했다는 긍정적인 결과를 발표했다. 근육손실을 나타내는 바이오마커인 마이오신(myosin)을 통해 근육생검 측정결과, 기준치 대비 근육손실이 23% 감소했던 것. 22명 환자 중 14명에서 마이오신이 감소했으며 유트로핀 중간값 수치는 기준치 대비 7% 증가했다. 즉, Ezutromid가 근육손실을 막고 유트로핀 수치를 증가시킴으로써 긍정적인 효과를 보인 것. 그러나 Ezutromid의 임상2상 최종결과, 약물의 내약성은 우수했지만 다리근육을 관찰한 MRI 수치가 기준치를 벗어나면서 2차 종결점을 충족하지 못했다.
Summit은 비용절감을 위해 선택과 집중 행보를 보이고 있다. Glyn Edwards 대표는 “유트로핀 조절제인 Ezutoromid가 DMD치료에 효과가 있을 것으로 기대했지만 실망스럽게도 DMD 환자에게 임상적으로 효능이 없었다. 우리는 DMD 임상개발을 중단하고 앞으로 새로운 기전의 C. difficile 항생제 파이프라인 ‘Ridinilazole’에 더 집중할 계획”이라고 밝혔다. Ridinilazole의 임상3상은 2019년 1분기 시작할 예정이다.
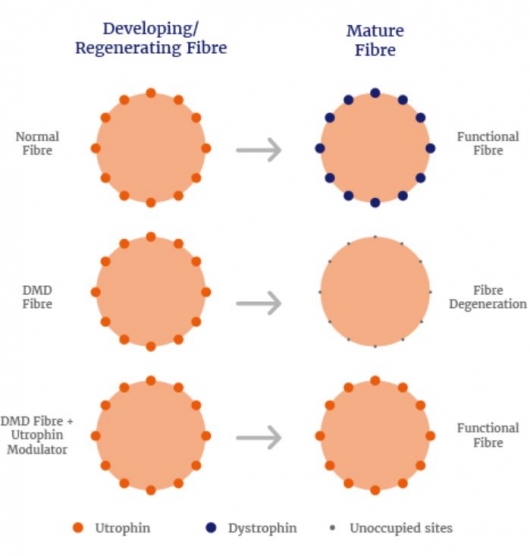
▲Summit Therapeutics의 DMD 신약후보물질 'Ezutromid'의 작용기전. (홈페이지 참조)
지난 2016년 Summit은 Ezutromid 및 유트로핀 조절제의 유럽, 터키, 독립국가연합 지역에 대한 독점적 권리를 사렙타 테라퓨틱스(Sarepta Therapeutics)에 기술수출하고 4000만달러 계약금(upfront)를 받았다. 임상2상에서 마지막 환자 투약시 2200만달러를 지급받고 로열티를 높이는 조건을 포함해 최대 5억2200만달러의 마일스톤 및 판매 로열티를 받을 수 있는 계약이었다.
Ezutromid의 임상실패로 사렙타 역시 실망스러운 입장이지만, DMD 치료제 개발연구는 계속되고 있다. 최근 사렙타는 DMD 신약후보물질 의 긍정적인 예비 임상1/2상 데이터를 공개했다. 환자 3명의 생검을 관찰한 결과 마이크로디스트로핀(microdystrophin)이 높은 수준으로 생성되고, 근육손실 바이오마커로 혈청 크레아틴 키나아제(creatine kinase, CK)의 수치가 유의미하게 감소해 평균이 87%로 감소했다는 결과를 발표했다.


















