바이오스펙테이터 장종원 기자
유전자재조합의약품 임상시험 신속진입 지원
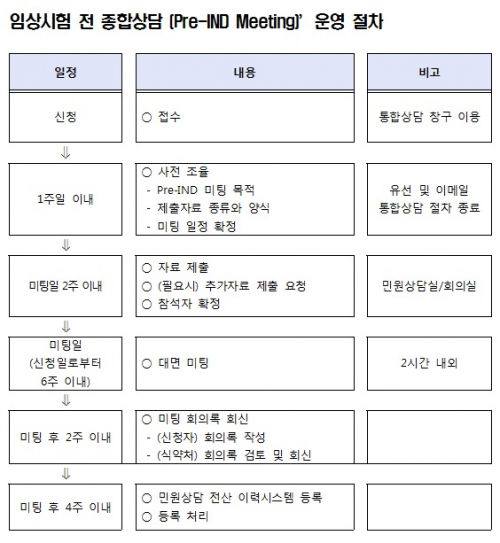
식품의약품안전처 식품의약품안전평가원이 신생 신약개발기업의 임상시험 신속 진입을 돕기위한 ‘임상시험 전 종합 상담(Pre-IND meeting)’을 운영한다. 기업들은 임상시험계획승인을 신청하기 전에 미리 개발계획, 제출자료, 임상시험계획 등에 대해 종합적으로 상담해 시행착오를 줄일 수 있다.
이번 종합상담은 유전자재조합의약품을 대상으로 시범운영하며 식약처 홈페이지 ‘통합상담 예약’을 통해 신청할 수 있다. 유전자재조합의약품은 유전자조작기술을 이용해 제조되는 펩타이드 또는 단백질 등을 유효성분으로 하는 의약품을 말한다.
대상은 6개월 이내에 임상시험 신청 계획을 갖고 있는 기업으로 ▲최초로 의약품 임상시험에 진입하는 업체 ▲최초로 유전자재조합의약품을 개발하는 업체 ▲국내에서 최초로 인간 대상 임상시험(FIH trial)을 계획하는 품목 등이 해당된다.
식약처는 또한 품목별로 개발단계에 맞는 품질, 비임상·임상계획 등에 대한 밀착상담 등 제품화를 지원하는 ’유전자재조합 맞춤형 협의체‘의 대상을 유전자재조합 신약에서 ’국내 개발 유전자재조합 전 품목‘으로 확대해 지원할 계획이다.