국제
포세이다, 시리즈C 1.42억弗 유치..“효율↑ CAR-T 개발"
바이오스펙테이터 서일 기자
Tscm비율↑, piggyBac DNA수정 기술 적용 CAR-T 세포치료제

미국 포세이다 테라퓨틱스(Poseida Therapeutics)는 노바티스(Novartis), Aisling Capital Management, Pentwater Capital Management, Perceptive Advisors, 미공개 투자자로부터 총 1억4200만달러의 시리즈 C 투자를 유치했다고 지난 22일(현지 시간) 발표했다.
포세이다는 P-BCMA-101 임상 1상(NCT 03288493) 결과를 지난해 12월 발표했다. 임상 1상은 23명의 재발성/난치성 다발성 골수종(Relapsed/refractory multiple myeloma) 환자를 대상으로 진행됐다. 종결점을 충족했으며, ORR이 100%로 확인됐다. 기존 CAR-T 세포 치료제보다 지속시간이 길게 나타났다. 2명의 환자에게서 CAR-T 세포 치료제 부작용으로 알려진 CRS(Cytokine Release Syndrome)가 발견됐지만, Grade 2 이하의 부작용이었다. 신경독성은 발견되지 않았다. P-BCMA-101은 FDA로부터 RMAT(Regenerative Medicine Advanced Therapy)로 지정된 바 있다.
포세이다는 Tscm(stem memory T cells) 비율, piggyBac DNA 수정(piggyBac DNA modification)으로 CAR-T 세포 치료제 한계로 지적되어왔던 반응 시간을 늘리고, 안전성을 높였다.
포세이다의 CAR-T 세포 치료제는 발생 초기 단계의 T 세포를 사용하여 기존 치료제보다 Tscm 세포 비율이 높다. Tscm 세포는 스스로 증식이 가능해, 기존 CAR-T 세포보다 체내 수명이 길다. 바이러스로 이미 분화된 T 세포를 조작하면 예상하지 못한 DNA 서열을 가진 Teff(effector T cells) 세포가 생겨나기도 한다. 포세이다의 CAR-T 세포는 Tscm이 Teff 세포로 분화하면서 Teff 세포 간의 동등성이 확보된다.
포세이다는 T 세포의 유전자를 수정하는 과정에서 바이러스가 아닌 piggyBac DNA 수정을 사용했다. piggyBac DNA 수정은 바이러스와 달리 Tscm 세포를 조작하는 것에 적합하다. piggyBac 트랜스포존(Transposon)을 사용하면 바이러스보다 많은 양의 DNA를 표적 지점에 정확히 넣을 수 있고, 바이러스를 이용한 CAR-T 세포 제작보다 비용, 시간을 줄일 수 있다. 바이러스 사용으로 생기는 독성 위험성을 줄일 수 있으며, 예상하지 못한 단백질을 표적하는 항체가 만들어지지 않는다.
포세이다는 CRISPR/Cas9, TALEN(Transcription activator-like effector nuclease)을 결합한 Cas-CLOVER를 이용하여 T 세포의 반응성을 높이는 연구도 진행 중이다.
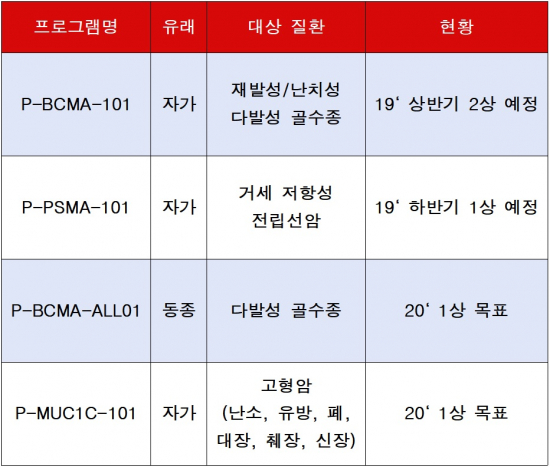
▲포세이다 CAR-T 세포 치료제 파이프라인(Poseida Therapeutics 홈페이지 참조, 바이오스펙테이터 재구성)




![[인사]한미그룹, 임원 승진 인사](https://img.etoday.co.kr/crop/74/74/2071974.jpg)









![[인사]한미그룹, 임원 승진 인사](https://img.etoday.co.kr/crop/77/77/2071974.jpg)



