오피니언
[이종혁 교수의 약가협상①]일본의 보험약가 등재제도
바이오스펙테이터 천승현 기자
제약사가 신약개발을 위한 R&D 투자를 결정하는데 있어서 가장 중요하게 고려하는 요소는 신약을 통하여 일정 수준의 수익성을 확보할 수 있는지의 여부라고 할 수 있다. 약가제도는 제약사가 R&D 투자를 결정하는데 있어서 중요한 요소로 작용할 뿐 아니라 환자의 신약에 대한 접근성에도 영향을 미친다.

▲이종혁 호서대 제약공학과 교수
우리나라의 약가제도는 고시가제도, 실거래가 상환제도, 시장형 실거래가 상환제도 등 의약품의 보험 상환방식의 제도변화와 함께 2006년「약제비 적정화 방안」으로 도입된 신약등재(의약품 선별등재 제도 및 약가협상 도입 등) 및 약가 사후관리제도(사용량-약가연동 협상제도, 급여범위 확대 시 약가인하 등)가 근간이 되어 현 제도에 이르게 됐다.
그러나「약제비 적정화 방안」시행 이후 건강보험 및 제약산업을 둘러싼 여러 가지 환경변화로 인하여 제도 도입 당시의 취지 및 목적 등이 현재 상황과는 배치되는 사례가 발생했다. 또한, 충분한 사전연구 없이 일부 새로운 제도를 도입하거나 기존 제도를 변경하여 제도간의 연계성 결여, 중복 또는 충돌이 발생하는 등 제도전반에 걸친 불신과 불만이 제약산업계에 팽배한 상황에 이르게 되었다. 또한, 너무나 다양한 약가 사후관리제도들이 복잡하게 얽혀 있어 제도에 대한 이해도, 예측성 및 수용성이 저하되어 문제점이 발생하기도 한다.
바이오스펙테이터는 보험약가 전문가 이종혁 호서대 제약공학과 교수의 기고를 통해 해외 약가등재와 사후관리 제도를 살펴보고 국내 약가제도의 개선책을 진단하고자 한다. 첫 회로 일본의 약가등재 제도를 소개한다.
1. 신약의 약가등재 절차
일본에서 시판허가된 의약품은 후생노동성 중앙사회보험의료협의회(중의협)의 심의를 거쳐 보험급여 의약품으로 선정된다. 중의협은 신약의 약가산정 절차를 투명하고 적정하게 하기 위하여 약가산정조직(Drug Pricing Organization, DPO)을 운영하고 있으며, 약가산정조직 회의를 통하여 개별 품목에 대한 약가산정안을 작성한다. 약가산정안 작성시 신청자가 의견을 제시할 수 있으며, 1차 약가산정안을 신청자가 수용하지 않을 경우 2차 약가산정조직회의에서 재검토하게 된다. 약가산정안 검토결과가 중의협에 통보되면 중의협 총회의 승인을 거쳐 의료보험 약가목록(NHI Drug Price List)에 등재된다. 신약의 등재 신청 후 등재까지 60일 이내 처리가 원칙이며, 늦어도 90일 이내에 처리되어야 한다. 약가등재 시기는 신약의 경우 1년에 4회(2,5,8,11월), 제네릭의약품은 1년에 2회(6,12월) 약가를 등재시킨다.
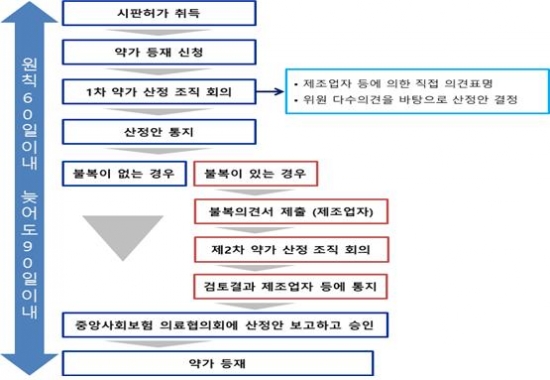
▲일본의 신약 약가 등재 절차
2. 신약의 가격결정방법
신약의 약가는 다음의 3단계를 거쳐 결정하게 된다.
□ Step 1 : 유사의약품이 있는 경우와 없는 경우로 나누어 각각의 방법에 따라 가격을 산정
① 유사의약품이 없는 경우 : 다음의 원가산정방식에 의함
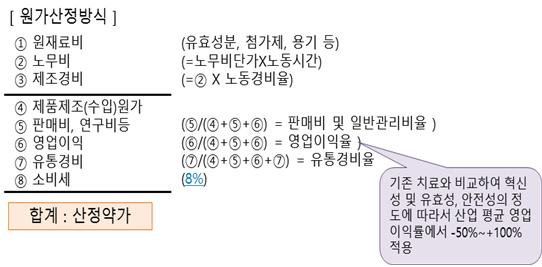
▲일본의 신약 약가결정 방법 (원가계산방식)
② 유사의약품이 있는 경우 : 획기성 등의 가산요인이 있는 신약과 신규성이 없는 신약으로 나누어 다음과 같이 산정한다.
- 유사약효비교방식(I) : 획기성 등의 가산요인이 있는 신약에 적용하는 방식으로 급여목록에 등재되어 있는 가장 유사한 의약품을 비교약으로 하여 신약의 1일약가를 기존 비교약의 1일 약가와 동일하게 산정한 후 획기성, 유용성, 시장성 등을 고려하여 가산을 적용하여 산정한다.이때 비교약은 원칙적으로 신약으로 등재된 지 10년이 지나지 않은 의약품으로 후발제품의 약가가 등재되어 있지 않은 제품을 선정한다.

▲일본의 신약 약가결정 방법 (유사약효 비교방식(I))
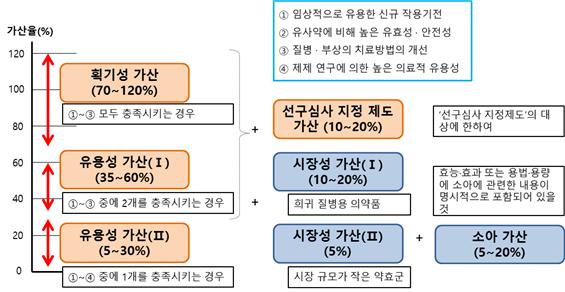
▲유사약효 비교방식(I)에 의하여 산정되는 신약의 가산의 종류 및 요건
- 유사약효비교방식(II) : 신규성이 없는 신약에 적용하며, 약리작용 유사약이 3개 이상 등재되어 있는 신약에 대해서는 신규성이 부족하다고 판단하여 보정가산을 적용하지 않으며, 과거 수 년 간 등재된 유사약제의 약가 중 가장 낮은 금액으로 산정한다. 유사약효 비교방식(Ⅰ)보다 낮은 수준에서 가격이 결정되며, 아래 두 가지 약가 중 낮은 가격으로 산정한다.

위에서 산정된 약가가 유사약효 비교방식(Ⅰ)에 의하여 산정된 약가보다 높을 경우 아래 2가지 약가 중 낮은 가격으로 산정한다.

□ Step 2 : Step 1에 따라 산정된 가격이 외국평균가격과 크게 차이가 날 경우 외국평균가격에 따라 조정함
- 유사약효 비교방식(Ⅰ), 유사약효 비교방식(Ⅱ) 또는 원가계산 방식으로 산정된 금액이 외국 가격과의 차이가 큰 경우에는 약가를 조정한다. 이 때 미국, 영국, 독일, 프랑스 가격의 평균을 외국 평균가격으로 한다.
- 유사약효 비교방식(Ⅰ) 과 원가계산 방식으로 산정된 경우 외국평균가격의 1.25배를 초과할 경우 가격을 인하하며, 0.75배 미만인 경우는 인상함
- 유사약효 비교방식(Ⅱ)에 의하여 산정된 경우 외국평균가격의 1.25배를 초과할 경우 가격을 인하하지만, 0.75배 미만이어도 인상하지 않음
□ Step 3 : 함량이 여러 가지일 경우 함량 간 가격조정을 거쳐 최종가격을 결정함
- 신약의 약가 산정 시 규격 간 조정방법은 아래와 같다.

이상의 일본의 신약의 약가결정 방법은 다음의 그림과 같이 간략히 나타낼 수 있다.
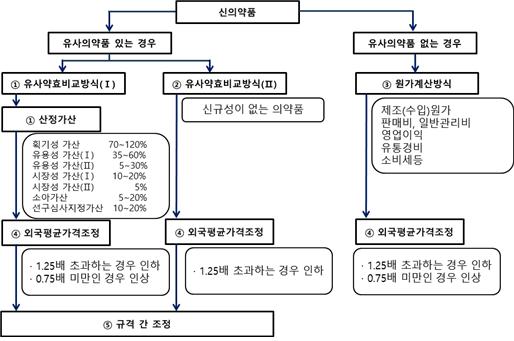
▲일본의 신약 약가결정 방법
3. 제네릭의약품의 약가등재
1) 약가산정방법
- 바이오의약품 외의 제네릭의약품의 약가는 특허만료된 오리지널의약품 약가의 50%로 산정하며, 제네릭의약품이 10개 이상인 경우에는 40%로 산정한다.
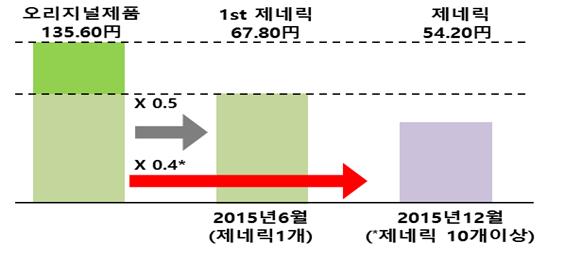
▲일본의 제네릭의약품 약가산정 기준
- 바이오 후발의약품의 경우는 오리지널의약품 약가의 70%(제네릭 제품 수가 10개 이상인 경우 60%) 로 산정하며, 승인신청 시 실시한 임상시험의 내용에 따라 최대 10%까지 가산하여 산정할 수 있다.
2) 기 등재 제네릭의약품의 약가조정
- 매 2년마다 실시하는 약가개정 시 조성, 제형 및 규격이 동일한 모든 유사의약품(제네릭의약품)에 대해서는 최고가의 30%미만일 경우(저가 약품군), 30%이상 50%미만일 경우(준 저가 약품군), 50%이상일 경우(기타 후발품군, 성분명으로 기재)의 3군으로 나누어 다음의 산식에 따라서 군별로 동일하게 약가를 산정하여 개정한다.

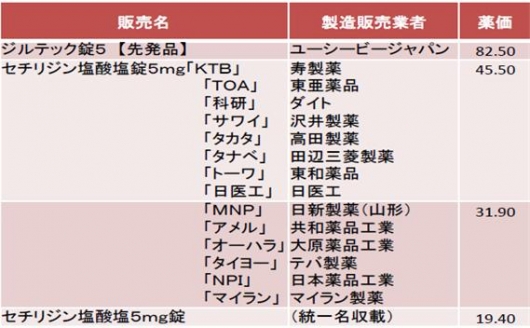
▲일본의 기 등재 제네릭의약품의 가격조정{자료 : 後発医薬品の薬価について (中医協, 平成27年10月28日)}


















