기업
‘확고한 캐시카우의 매력’..녹십자, 6년연속 매출 신기록
바이오스펙테이터 천승현 기자
혈액ㆍ백신제제 지속 상승세로 매년 안정적 성장세..작년 매출 중 57% 차지, 희귀질환치료제 등 새 수익원 가세
GC녹십자가 간판 사업인 혈액제제와 백신제제의 안정적인 성장세를 기반으로 6년 연속 매출 신기록을 냈다. 일정 규모의 매출이 보장된 수익원(캐시카우)을 보유하면서 영업이익도 지속 상승세를 나타냈다.
6일 금융감독원에 따르면 GC녹십자는 지난해 연결 재무제표 기준 영업이익이 903억원으로 전년동기대비 15.1% 늘었다. 같은 기간 매출액은 1조2879억원으로 전년보다 7.5% 증가했다. GC녹십자의 작년 매출액은 사상 최대 기록이며 지난 2012년부터 6년 연속 매출 신기록을 갈아치웠다.
연도별 GC녹십자의 실적을 살펴보면 매년 큰 기복없이 안정적인 상승세를 나타낸다는 큰 특징이 있다.
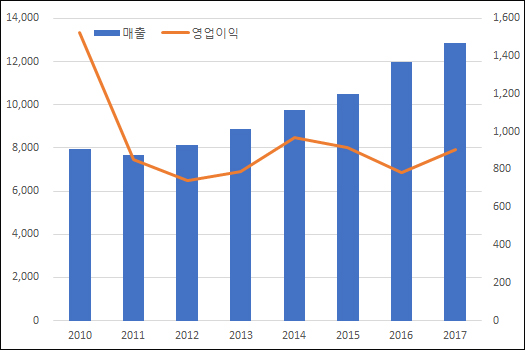
▲연도별 GC녹십자 매출·영업이익 추이(단위: 억원, 자료: 금융감독원)
GC녹십자는 지난 2010년 갑작스러운 신종플루의 유행으로 일시적인 실적 상승을 기록한 이후 2012년부터 매년 10% 안팎의 매출 성장률을 기록했다. 매출 성장률이 가장 낮은 2012년에도 5.7% 증가했고, 2016년에는 전년대비 14.3%의 성장률을 나타냈다.
영업이익도 매년 700억~900억원대로 꾸준한 수치를 지속했다. 매출액 대비 영업이익률은 6.6%(2016년)~11.1%(2011년)로 매년 유사한 수준을 보였다.
간판 사업부문인 혈액제제와 백신제제가 매년 지속적으로 안정적인 성장세를 나타낸 영향으로 분석된다.
지난해 GC녹십자의 매출액(1조2879억원)에서 혈액제제(4175억원)와 백신제제(3203억원)가 차지하는 비중은 각각 32.4%, 24.9%에 이른다. 혈액제제와 백신제제가 전체 매출의 57.3%를 차지한다는 의미다.
혈액제제와 백신제제 모두 매년 안정적인 상승흐름을 지속하고 있다. 혈액제제의 매출은 2011년 3063억원에서 지난해 4175억원으로 36.3% 늘었고, 같은 기간 백신제제는 1185억원에서 3203억원으로 170,3% 증가했다.
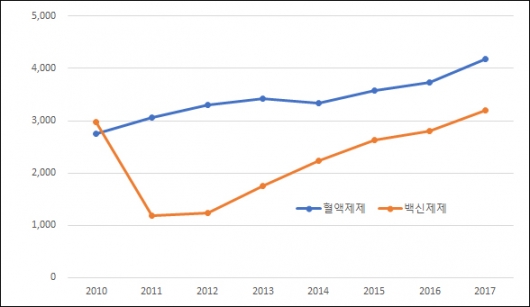
▲연도별 GC녹십자 혈액·백신제제 매출 추이(단위: 백만원, 자료: 금융감독원, GC녹십자)
주요 혈액제제 품목별 매출을 보면 지난해 ‘알부민’이 국내외 시장에서 832억원어치 팔렸고 면역글로불린 '아이비글로불린-에스엔’(IVIG-SN)은 838억원의 매출을 기록했다. IVIG-SN의 경우 국내(200억원)보다 수출 실적(638억원)이 월등히 많았다. GC녹십자는 지난해 말 브라질 정부 의약품 입찰에서 4290만달러 규모의 ‘IVIG-SN'을 수주하며 혈액제제의 해외 수주 규모도 늘려가고 있다.
백신제제는 독감백신이 지난해 1036억원의 매출을 기록했다. 국내(520억원)와 해외(516억원)에서 모두 500억원 이상의 매출을 올렸다. GC녹십자는 2010년부터 세계보건기구(WHO) 산하기구 등을 통해 독감백신의 수출을 진행 중인데 누적 수주액은 2억달러를 넘어섰다. 지난해에는 남반구 의약품 입찰에서 약 3700만달러 규모의 독감백신을 수주한 바 있다.
대상포진백신 ‘조스타박스’(931억원), 자궁경부암 백신 ‘가다실’(510억원) 등 다국적제약사가 개발한 도입신약의 매출이 가세하면서 백신제제 사업 영향력도 확대됐다.
GC녹십자가 자체개발한 희귀질환치료제 ‘헌터라제’가 지난해 279억원의 매출을 기록했다는 점도 눈에 띄는 대목이다. 지난 2012년 국내 허가를 받은 헌터라제는 세계에서 두 번째로 개발된 헌터증후군 치료제다.

▲GC녹십자 헌터증후군치료제 '헌터라제'
‘2형 뮤코다당증’으로 불리는 헌터증후군은 남아 10만~15만 명 중 1명의 비율로 발생하는 것으로 알려진 희귀질환이다. 선천성 대사 이상 질환인 헌터증후군은 골격이상, 지능 저하 등 예측하기 힘든 각종 증상을 보이다가 심할 경우 15세 전후에 조기 사망하는 유전병이다. 국내 환자 수는 70~80명 가량에 불과하다.
헌터라제는 세포배양 방식으로 생산한 효소를 환자에게 주사하는 방식으로 헌터증후군 증상을 개선하는 효능이 있다.
세계적으로 헌터증후군 치료제는 미국 샤이어의 '엘라프라제' 1개밖에 없어 기존 치료제의 공급에 문제가 생길 경우 환자 치료에 지장을 초래하는 문제가 지적됐다. 헌터라제가 엘라프라제의 독점구조를 무너뜨린 것이다.
헌터라제는 투여 환자 수는 많지 않지만 희귀질환치료제 특성상 비싼 가격으로 책정되면서 판매량이 많지 않지만 고수익을 가져왔다. 헌터라제는 현재 중남미와 북아프리카에서도 판매되는데 지난해 해외에서만 102억원어치 팔렸다.
GC녹십자는 미국, 일본 등 선진 의약품 시장을 정조준 한 상태다. 미국에서는 지난 2013년 희귀의약품(Orphan Drug)으로 지정받고 임상2상시험을 진행 중이다. 희귀의약품으로 지정되면 임상시 최대 50% 세금감면과 신속심사, 허가비용 감면 등 혜택이 주어진다. 일본에서는 헌터라제를 정맥주사가 아닌 뇌에 직접 투여하는 약물로 개발하기 위해 임상시험을 전개 중이다.
GC녹십자는 올해 IVIC-SN의 본격적인 미국 진출을 기대하고 있다. GC녹십자는 2015년 11월 FDA에 제출한 IVIG-SN의 생물학적제제 품목허가 신청서에 대한 검토완료공문을 통해 제조공정 관련 자료의 보완을 지적받았다. 이에 FDA로부터 지적받은 제조공정을 개선하고 최종 승인 절차를 거쳐 올해에는 IVIG-SN의 최종 승인이 예상된다. 이미 GC녹십자는 북미 생산거점으로 캐나다에 약 2200억원을 투입해 혈액분획제제 생산시설을 건설하는 등 미국시장 진출 채비를 마친 상태다.

▲캐나다 퀘벡 주 몬트리올광역시에 위치한 GC녹십자 캐나다 법인 GCBT의 혈액제제 공장 전경
미국 시장 진출을 포기한 혈우병치료제도 약효 지속시간을 늘린 차세대 제품을 개발 중이다. GC녹십자는 목암생명과학연구소와 공동으로 차세대 혈우병A형치료제 ‘MG1121’을 개발 중인데 비임상 시험에서 반감기가 기존 제품 대비 3배 이상 늘어났다는 연구결과를 최근 미국 혈액학회 연례회의에서 발표했다.
GC녹십자 관계자는 “올해에도 전사적 경영 효율화를 통해 내실을 강화하고 지속성장의 기반을 위한 과감한 미래투자를 계획하고 있다”고 말했다.



















