오피니언
서정진 "코로나 항체신약 9월 생산..내년 상반기 허가"
바이오스펙테이터 장종원 기자
9월부터 상업생산 시작..2상 후 긴급사용승인 신청..변이 대비한 후속 항체신약도 개발 돌입
서정진 셀트리온그룹 회장이 20일 "내년 상반기까지 코로나19 항체 치료제를 허가받는 것이 목표"라고 밝혔다. 셀트리온은 이를 위해 이달부터 'CT-P59'의 국내외 임상을 빠르게 진행할 계획으로, 오는 9월부터는 송도 공장에서 상업생산에도 돌입한다. 신종코로나바이러스 변이에 대응할 수 있는 후속 항체 치료제 파이프라인 개발도 뒤따르고 있다.
서 회장은 이날 온라인 기자간담회를 통해 셀트리온의 코로나19 항체 치료제 개발 상황을 설명했다.
식품의약품안전처는 지난 17일 셀트리온 코로나19 항체 치료제 CT-P59의 임상시험계획을 승인한 바 있다. 충남대병원에서 건강함 피험자 32명을 대상으로 진행하는 1상이다.
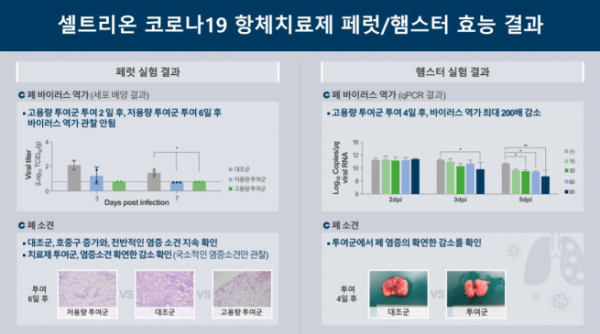
서 회장은 "1상은 금주 피험자 투여를 시작해 1~1.5개월 진행하고 곧바로 2상(200~300명 규모), 3상(2000~3000명 규모)으로 진입할 계획"이라면서 "올 연말까지 한국과 유럽 몇개 국가에서 임상을 진행할 예정"이라고 설명했다. 임상은 코로나19 경증환자와 중등증 환자를 대상으로 하며 특히 CT-P59의 코로나19 효능뿐 아니라 예방효과를 확인할 수 있는 프로토콜로 진행할 계획이다.
서 회장은 "임상 2상에서 도출된 결과에서 안전성과 유효성이 확인되면 긴급사용승인도 신청할 계획"이라면서 "내년 상반기까지 모든 임상과 허가를 끝내는 것이 목표"라고 설명했다.
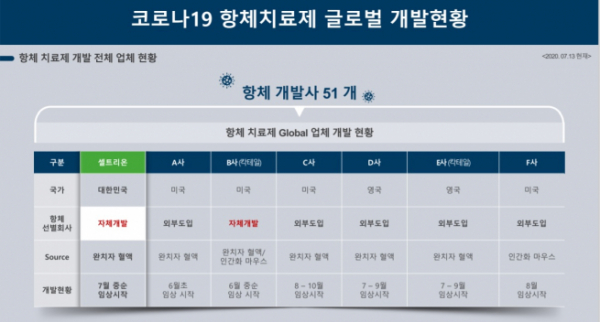
셀트리온이 자체 파악한 바에 따르면 현재 코로나19 항체 치료제 글로벌 개발사는 50여곳에 달한다. 이달 중순 임상에 돌입하는 셀트리온은 속도면에서는 선두그룹에 속한다.
서 회장은 코로나19 항체 치료제의 성패는 효능과 안전성을 넘어 가격이 좌우할 것이라고 단언했다. 그는 "항체는 제조원가가 비싸기 때문에 전세계에 저렴하게 공급하는 것이 관건"이라면서 "셀트리온은 개발비와 제조비용을 최대한 낮춰 어느 회사보다도 저렴하게 가격을 책정할 것"이라고 밝혔다.
셀트리온은 CT-P59의 허가에 앞서 사전 생산을 통해 물량을 확보할 계획이다. 서 회장은 "오는 9월부터 인천 송도 공장에서 연간 생산능력 280배치 중 10배치 정도를 배정해 상업 생산을 시작할 것"이라며 "2상 이후 긴급사용 승인을 획득하게 되면 환자들에게 즉시 투입이 가능하다"고 밝혔다. 셀트리온은 생산능력 확대를 위해 전세계 CMO와도 협의하고 있다고 덧붙였다.
셀트리온은 이날 신종코로나바이러스에 대응하기 위한 프로젝트도 가동하고 있다고 소개했다. 현재 코로나19 바이러스를 구성하는 3만개의 염기서열 중 1352개 아미노산이 변경돼 5786개 타입 변이가 발생했다. 하지만 현재 개발 중인 코로나19 치료제(S1타깃)나 백신을 무력화 할 정도의 변이는 아니라는 설명이다.
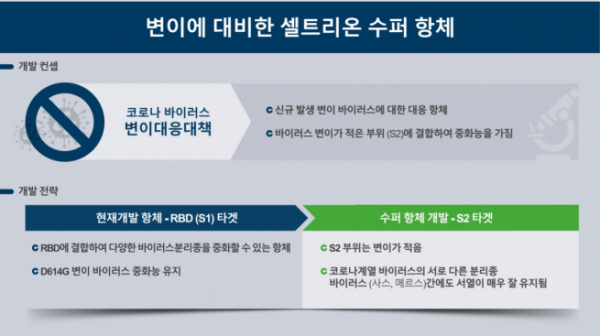
셀트리온은 그럼에도 불구하고 바이러스변이가 적은 부위(S2)에 결합해 중화능을 가진 새로운 항체를 개발하고 있다. S2를 타깃하는 항체 개발은 셀트리온과 제넨텍 등 일부 회사만 진행한 프로젝트라는 게 서 회장의 설명이다. 그는 "S1을 타깃하는 CT-P59와 동시에 S2 타깃 후속 코로나19 항체치료제도 6개월차를 두고 개발하고 있다"고 소개했다.
한편 서 회장은 올 연말 은퇴하겠다는 기존 입장을 유지했다. 그는 "연말까지는 직접 지휘하면서 제품을 개발하지만 연말이 지나면 후배들이 지휘할 것이다. (셀트리온이) 회장이 있으면 개발이 잘되고, 회장이 물러나면 안 될 정도로 허약한 회사가 아니다"며 "우리 회사 임직원의 실력을 믿어 달라"고 말했다.


















