기업
프론트바이오, '당뇨약 복합제' 항암효과 연구논문 게재
바이오스펙테이터 서윤석 기자
제2형 당뇨병 치료제 '메트포르민'+'아피제닌' 복합제..암세포 선택적 활성산소(ROS) 증폭 기전..종양 마우스모델서 암크기, 암무게 감소

프론트바이오는 개발 중인 복합제를 이용한 세포∙동물모델에서의 항암효과 연구결과를 국제학술지 ‘사이언티픽 리포트(Scientific reports)’에 게재했다고 13일 밝혔다(doi.org/10.1038/s41598-021-93270-0).
논문에 따르면 프론트바이오는 '메트포르민(metformin)'과 '아피제닌(apigenin)'을 조합해 종양세포 특이적으로 활성산소(reactive oxygen species, ROS)를 높인 항암제를 개발 중이다.
프론트바이오는 췌장암 세포(AsPC-1)와 정상세포(human primary dermal fibroblast, HDF)에 메트포르민/아피제닌을 투여한 결과 암세포에서만 ROS 증가를 통한 세포사멸 등을 확인했다. 또 AsPC-1 세포를 이식한 종양 마우스 모델에 메트포르민/아피제닌을 투여한 결과 종양크기(tumor volume) 및 종양무게(tumor weight)가 감소한 결과를 보였다.
메트포르민은 제2형 당뇨병 환자의 혈당을 조절하는 약물로 사용되고 있다. 메트포르민은 독소루비신(doxorubicin), 시스플라틴(cisplatin), 트라메티닙(trametinib) 등의 항암제와 조합해 다양한 종양을 가진 모델동물에 투여했을 때 항암효과를 보였다고 알려져 있다.
아피제닌(4′,5,7-trihydroxy-favone)은 각종 과일 및 채소류에 있는 플라보노이드(flavonoid)의 일종으로 세포내 ROS(intracellular ROS)를 증폭시킨다. 아피제닌은 젬시타빈(gemcitabine) 등의 항암제와 조합해 세포 및 동물모델에서 항암효과를 나타냈다고 알려져 있다.
먼저 연구팀은 메트포르민/아프제닌을 췌장암세포주인 AsPC-1과 정상세포주인 HDF에 투여했다. 그 결과 AsPC-1 세포에서 DNA 손상마커인 p-ATM, γ-H2AX 등과 세포사멸(apoptosis) 마커인 p-p53, Bim, caspase3 등이 유의미하게 증가한 결과를 확인했다(p<0.05). 또 자가포식(autophagy) 마커인 LC3B, AIF 등과 네크롭토시스(necroptosis) 마커인 MLKL, p-MLKL, p-RIP3 등의 발현도 증가했다. 그러나 정상세포주에서는 이런 바이오마커들이 변화하지 않았다.
연구팀은 AsPC-1을 이식한 동물모델에서 메트포르민/아피제닌의 항암효과를 확인했다. 구체적으로 메트포르민75mg/kg+아피제닌 5mg/kg을 경구투여한 AsPC-1 마우스모델은 각각을 투여했을 때보다 종양크기를 약 1000㎣에서 약 400㎣으로 감소시켰다. 종양 무게도 약 400mg에서 약 300mg으로 유의미하게 줄였다. 이런 효과는 메트포르민과 아피제닌을 각각 125mg/kg, 40mg/kg으로 높였을 때 더 효과적으로 나타났다.
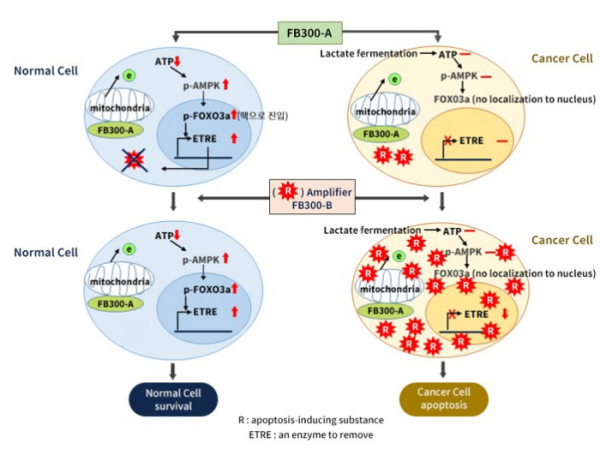
프론트바이오는 이번 연구를 통해 암세포 선택적인 ROS 증폭(cancer cell specific ROS amplification, CASRA) 기전을 규명했다는 설명이다.
이재용 프론트바이오 대표는 "활성산소 증폭을 통해 암세포만 선택적으로 사멸시킬 수 있는 기전의 항암제를 개발 중이다"며 "기존 항암제가 가지고 있는 부작용을 최소화시키고 치료 효율을 높인 약물을 개발할 것"이라고 말했다.
한편, 프론트바이오는 2022년 상반기에 CASRA 기전의 항암제 임상1상 진입을 목표로 연구를 진행 중이다.
(프론트바이오 홈페이지 참조)



















