BioS+
[이종혁 교수의 약가협상③]대만의 보험약가제도
바이오스펙테이터 천승현 기자
가. 신약의 등재절차
대만의 건강보험은 우리나라와 같이 단일보험자로 전 국민이 가입되어 있다. 건강보험의 운영은 위생복리부(Ministry of Health and Welfare, 이하 MOHW)가 주관하고 있으며, 중앙건강보험서(National Health Insurance Administration, 이하 NHIA)에서 운영한다.
제약사가 NHIA에 임상시험자료 및 경제성평가 자료와 함께 급여결정신청을 하면 신약의 등재절차가 시작된다. NHIA는 의약품 검증센터(Center for Drug Evaluation, CDE)내의 Health Technology Assessment(HTA)와 Advisory meeting 에서 신청약제의 임상적 유용성과 비용효과성, 재정영향 등을 평가하여 1차적으로 가격 및 등재여부를 결정한다. 그 후 약제평가위원회(Pharmaceutical Benefits and Reimbursement Schedule Joint Meeting, 이하 PBRS Joint Meeting)에서 합의가 이루어지면 제약사와 NHIA의 협상을 통하여 급여목록에 등재된다.
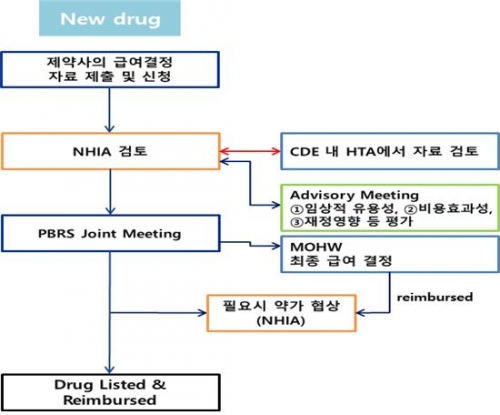
▲대만의 보험약가 등재절차
2013년 1월부터 PBRS jonit meeting이 신설되었는데, 이는 NHIA내의 전문평가위원회로 2개월마다 개최되어 약가 등재여부와 가격, 급여기준을 평가한다. 위원회의 위원은 각계 전문가 및 이해관계자 30명으로 구성되며, 제약산업계 대표 3명을 배석할 수 있도록 하여 위원회의 투명성을 강화한 것이 특징적이라 할 수 있다. (그림 5-4 참조) 회의결과에 대하여 제약사의 이의가 있을 시 다음 회의에 재상정할 수 있으며, 회의내용을 NHIA 웹사이트에 공지한다.... <계속>



















