기업
의약품 재평가 결과 26개 ‘유용성 불인정’..시판금지
바이오스펙테이터 천승현 기자
식약처, 2016년 재평가 결과 공시..'스트렙토키나제·스트렙토도르나제' 성분 66개 임상 재실시
식품의약품안전처는 항생제, 비타민제, 자양강장변질제 등 9개 분류군 6736개 품목에 대한 2016년 재평가 결과 26개 품목에 대한 유용성이 불인정된다고 판단, 시판금지한다고 16일 밝혔다.
시판금지 대상은 삼오제약의 ‘살프메칠렌블루주사1%’, 서흥의 ‘하이클린정’, 서울약품의 ‘토코라민지’, 알보젠코리아의 ‘폴리비탄주’, 한올바이오파마의 ‘아미노젠정’ 등이다.
유용성이 불인정되는 품목은 허가 받은 효능·효과, 용법·용량 등에 대한 안전성·유효성을 현재 과학수준에서 입증할 수 있는 충분한 자료가 제출되지 않다는 판단에 재평가 결과 공시일로부터 회수·폐기하고 시판금지한다.
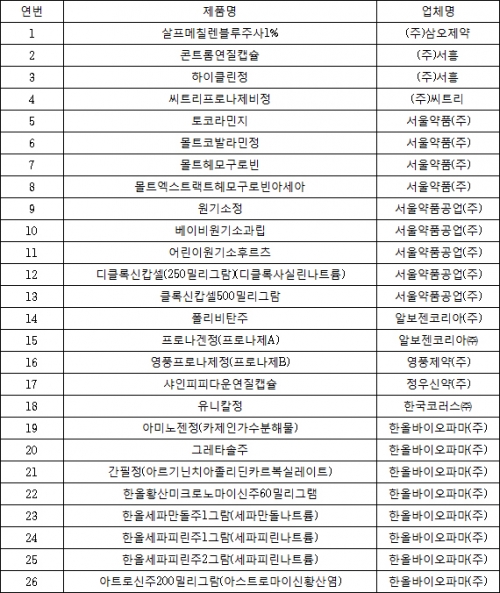
▲의약품 재평가 결과 유용성 불인정 26개 품목(자료: 식품의약품안전처)
이와 함께 식약처는 염증성 질환 등에 사용하는 스트렙토키나제·스트렙토도르나제 함유 66개 품목은 효능·효과 입증을 위한 임상시험을 추가로 실시하도록 지시했다. 한미약품, JW중외제약, 안국약품, 휴온스 등이 임상 재실시 대상이다.
식약처는 이번 재평가 대상 6736개 품목 중 5706개 품목은 허가사항을 유지키로 결정했고, 938개 품목은 허가사항의 일부를 변경키로 했다.
허가사항이 변경되는 품목은 임상시험 자료, 미국, 유럽, 일본 등 외국 사용현황 등을 토대로 효능·효과, 용법·용량, 복용 시 주의사항 등을 변경했다.
‘우르소데옥시콜산’ 50mg과 비타민이 함유된 대웅제약의 ‘대웅우루사연질캡슐’ 등 14개 품목은 기존 효능·효과인 ‘만성간질환의 간기능개선, 간기능장애에 의한 전신권태, 소화불량, 식욕부진, 육체피로’ 에서 ‘소화불량과 식욕부진’은 삭제된다.
패혈증 등에 사용하는 ‘세포테탄’ 성분의 항생제는 소아에 대한 용법·용량이 삭제된다. 제일약품의 ‘야마텐탄주1그람’ 등 28개 품목이 해당된다. 골연화증에 사용하는 칼시트리올제제(한국로슈 ‘로칼트롤연질캡슐0.25마이크그람’ 등 5개 품목)는 모유 중으로 이행 가능성이 있어 수유부에 투여시 주의해 사용하도록 했다.
평가 결과에 따라 허가사항 변경이 필요한 품목은 결과공시일로부터 1개월 이내에 허가변경을 해야 하며, 변경 허가일 이후 출고되는 모든 제품에는 변경내용을 반영해 유통해야 한다.
식약처 관계자는 “이번 재평가 결과를 통해 안전성·유효성이 확보된 의약품이 공급될 뿐 아니라 의약품을 안전하게 사용하는데도 도움이 될 것”이라며 “앞으로도 시판 후 의약품 안전관리에 강화를 위해 노력하겠다”고 말했다.



















