기업
이앤에스, 유방암 진단 연구결과 공개.."올해 허가임상"
바이오스펙테이터 장종원 기자
혈액 기반 ‘DxMe® BC’, 2018년 4차례 검증서 민감도·특이도 '95% 이상'..유방조영술 보완재로서의 가능성도 확인

이앤에스헬스케어가 혈액 기반의 유방암 조기진단키트 ‘DxMe® BC’의 질환 예측력을 담보할 새로운 연구결과를 공개했다. 이 키트는 수차례 성능 검증에서 일관되게 90% 이상의 민감도와 특이도를 기록해 기존 유방조영술을 보완하는 진단으로서의 가능성을 보였다. 이앤에스헬스케어는 올해 국내 식품의약품안전처 품목허가를 위한 확증 임상시험에 돌입할 예정이다.
서경훈 이앤에스헬스케어 대표는 최근 KAIST 기업가정신연구센터가 주최한 '벤처 스타트업 서밋'에서 'DxMe® BC'를 검증한 각종 연구결과를 내놨다.
2013년 서경훈 대표가 창업한 이앤에스헬스케어는 활성산소(Reactive oxygen species)에 대항하는 항산화 단백질 Thioredoxin1(Trx1)을 바이오마커로 활용한 유방암 조기진단 키트 'DxMe® BC'를 개발했다. Trx1 마커는 2007부터 2013년까지 운영된 지식경제부의 시장선도형분자세포진단제개발사업단의 성과물이기도 하다.
엘라이자(ELISA) 기반의 'DxMe® BC'는 정상인 100명과 유방암 환자 100명의 혈액 샘플을 이용한 초기 연구결과에서 95% 이상의 높은 민감도와 특이도를 확인했다. 기존 유방암 예후 진단 목적으로 사용되는 제품 CA15-3의 민감도(48%), 특이도(70.4%)를 크게 상회하는 결과다. 민감도는 환자를 환자로 판별할 수 있는 능력, 특이도는 정상인을 정상인으로 판별할 수 있는 능력을 말한다.
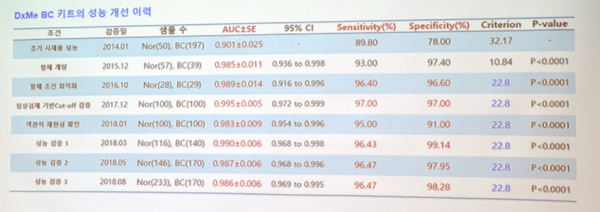
이앤에스헬스케어는 지난해 4차례의 성능검증 연구를 통해 민감도와 특이도를 재확인했는데 모두 96% 이상의 결과를 보였다. 현재까지 정상인 259명과 유방암환자 190명을 검증한 결과는 민감도 94.7%, 특이도 98.1% 였다. 양성으로 판정된 피검사자가 실제로 양성일 확률인 양성예측도는 97.3%, 음성으로 판정된 피검사자가 실제로 음성일 확률인 음성예측도는 96.2%로 나타났다.
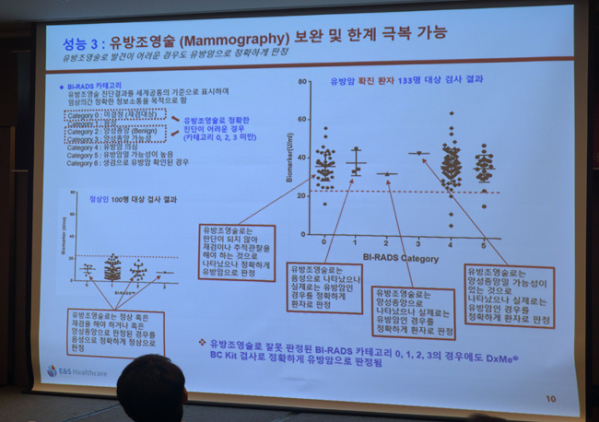
이앤에스헬스케어는 현재 유방암 진단법인 유방조영술(Mammography)와 비교한 연구결과도 공개했다. 유방암 확진환자 133명의 유방조영술 결과 ▲유방조영술로는 판단이 되지 않거나 ▲유방조영술로 음성이 나타나거나 ▲유방조영술로는 양성종양으로 나타난 경우를 'DxMe® BC'는 정확하게 유방암으로 판정했다. 반대로 정상인 100명을 대상으로 유방조영술로는 정상 혹은 재검을 해야 하거나 양성으로 판정된 경우에도 'DxMe® BC' 정상으로 판정했다. 서 대표는 "이앤에스 키트가 유방조영술을 보완해 유방암을 진단하는 가능성을 보여준 연구결과"라고 소개했다.
특히 이 키트는 유방암에서 유전자형, 병기, 나이 등과 관계없이 일관되게 진단이 가능한 연구결과를 보였다. 유방암 환자의 샘플을 연령에 따라 분류해 진행한 실험에서도 일정하게 환자 선별이 가능했으며 폐경과 같은 여성의 생리학적 환경에도 영향을 받지 않는 것을 확인했다. 또한 조직학적 병기와 세포 증식률 뿐만 아니라 Estrogen 수용체, Progesteron 수용체, HER2 등 각기 다른 유전자형도 관계없이 진단이 가능했다.
또한 Trx1 마커는 유방암에서만 높은 발현을 보여 우수한 유방암 구별 능력을 보였다. 다만 서 대표는 "자궁경부암의 경우 Trx1 평균값이 유방암 진단의 Cut-off 값 위로 나타나나 자궁경부암 발생률은 유방암 발생률의 18.7% 밖에 되지 않아 실제 진단 현장에서 유방암과 혼돈될 가능성이 낮다"고 설명했다.
서 대표는 "전세계 많은 기업이 대규모 투자 유치를 통해 유방암 조기진단 개발에 나섰으나 실패를 거듭했다. 'DxMe® BC'는 혈액기반의 퍼스트인클래스 제품"이라면서 "유방조영술을 보완하는 것부터 치료후 환자관리까지 다양하게 활용할 수 있을 것"이라고 설명했다. 이앤에스헬스케어는 식품의약품안전처와 협의를 통해 올해 국내 품목허가를 위한 확증임상에 돌입할 계획이다. 미국, 유럽, 동남아시아, 남미 등 글로벌 시장 진출도 모색하고 있다.















