국제
릴리, 'PEG IL-10 약물+PD-1' 병용 1b상 결과공개
바이오스펙테이터 이승환 기자
페길레이션 기술 적용해 작용시간 늘린 페길화 IL-10 ‘페길로데카킨’..객관적반응률(ORR) 신세포암종 40%, 비소세포폐암 43%, 흑색종 10% 확인

일라이릴리(Eli Lilly)의 지속형 IL-10 수용체 작용제 ‘페길로데카킨(pegilodecakin, PEGylated IL-10)’을 면역항암제와 병용한 임상1b상(IVY, NCT02009449) 결과가 공개됐다.
MD 앤더슨 암센터(MD anderson cancer center) 연구진은 악성종양을 가진 진행성 고형암 환자 111명에게 ‘페길로데카킨+PD-1 항체’ 병용요법을 투여한 IVY 연구 결과를 지난 25일(현지시간) 국제학술지 ‘란셋 온콜로지(Lancet Oncology)’에 게재했다(doi: 10.1016/S1470-2045(19)30514-5).
111명의 IVY 연구 참여 환자 중 38명은 신세포암종(renal cell carcinoma, RCC), 37명은 흑색종(melanoma), 34명은 비소세포폐암(non-small-cell lung cancer, NSCLC)을 앓고 있었다. 1명은 삼중음성유방암(triple-negative breast cancer, TNBC), 나머지 1명은 방광암(bladder cancer)을 앓고 있었다. 111명은 2개의 그룹으로 나뉘었으며, 53명은 ‘키트루다(Keytruda, 성분명: pembrolizumab)’, 58명은 ‘옵디보(Opdivo, 성분명: nivolumab)’를 페길로데카킨과 병용투여했다.
페길로데카킨, 면역항암제 병용투여로 발생한 Grade 3, Grade 4 부작용은 111명 중 73명에게서 나타났다. 73명 중 35명은 키트루다, 38명은 옵디보를 투여받았다. IVY 연구의 주요 부작용은 빈혈, 혈소판감소증, 피로감, 고중성지방혈증이며, 치명적인 부작용은 확인되지 않았다. IVY 연구에서 종양의 축소가 나타난 객관적반응(objective responses, OR) 환자 수는 신세포암종 35명 중 14명(40%), 흑색종 31명 중 3명(10%), 비소세포폐암 28명 중 12명(43%)이었다.
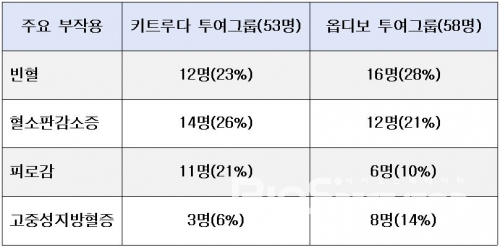
▲IVY 연구 주요 부작용 발생 수(doi: 10.1016/S1470-2045(19)30514-5, 바이오스펙테이터 정리)
페길로데카킨은 페길레이션(pegylation) 기술을 적용한 IL-10으로, IL-10에 폴리에틸렌 글리콜(polyethylene glycol, PEG)을 결합했다. 약물은 흡수-분포-대사-제거 총 4단계를 거쳐 작용하는데, 페길레이션은 약물의 대사, 제거 정도를 낮추어 약물이 체내에 머무는 시간을 늘린다. 체내에 머무는 시간이 늘어난 약물은 작용시간이 상대적으로 증가하기 때문에 약물의 효율이 높아진다.
페길로데카킨은 일반적인 IL-10보다 체내에 길게 머무르며, Th1세포, CD8+ T세포 활성을 높이고 수를 증가시킨다. 그리고 IFN-γ 발현을 높여 Tc1세포의 퍼포린(perforin), 그랜자임B(granzyme B) 분비량을 높인다. 이를 통해 CD8 T세포의 항암 반응을 유도하는 것으로 알려졌다(doi: 10.1089/jir.2014.0221).
일라이릴리는 2018년 5월 아르모 바이오사이언스(ARMO BioSciences)를 인수하는 계약에 합의하면서 페길로데카킨을 파이프라인으로 확보했다. 일라이릴리는 아르모의 주식을 주당 50달러로 책정해 16억달러 규모 계약을 체결했다. 일라이릴리가 아르모를 인수할 무렵에 아르모는 페길로데카킨을 진행성 췌장암 환자에게 투여하는 임상3상(SEQUOIA, NCT02923921)을 진행하고 있었다. SEQUOIA 연구결과는 2020년에 공개될 예정이다.
한편 지난 2015년 한미약품이 사노피(Sanofi), 얀센(Janssen)에 각각 39억유로(약 5조원), 9억1500만달러(약 1조원) 규모 기술이전 계약을 체결했던 당뇨, 비만 치료제도 약물의 효율을 높인 치료제다. 한미약품의 플랫폼 기술 가운데 하나인 ‘랩스커버리(LAPSCOVERY)’는 비당쇄화된 면역글로불린(aglycosylated Fc)을 약물에 결합해 약물의 대사, 제거 정도를 낮추는 방식으로 약물의 효율을 증가시킨다.















