국제
암젠, BCMA BiTE 초기 임상1상 공개.."sCR 관찰"
바이오스펙테이터 김성민 기자
재발/불응성 환자 고용량 BCMA X CD3 BiTE 'AMG 420' 투여군...sCR 5명, 4명 MDR(-), 10개월 이상 반응 지속 "셀진/블루버드 bb2121 등 BCMA CAR-T와 경쟁구도 예상"
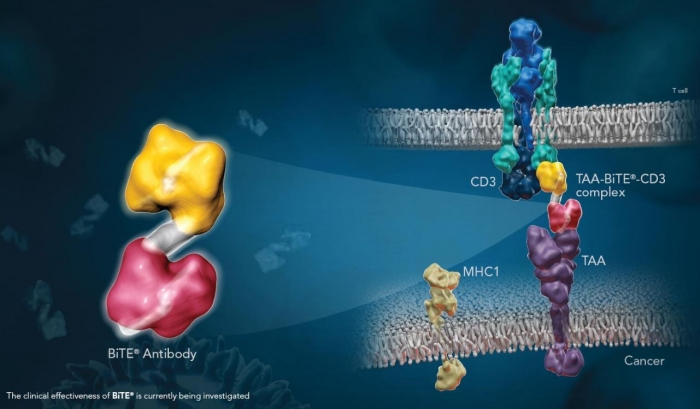
▲종양 타깃으로 T세포를 끌어들이는 BiTE, 암젠 자료 참조
T세포를 타깃한 이중항체가 수억 원에 이르는 CAR-T 치료제에 해결책을 제시할 수 있을까? 다발성골수종에서 BCMA(B-cell maturation antigen) 타깃 CAR-T 개발 경쟁이 치열해지고 있는 상황에서, 암젠의 BCMA 이중항체(BiTE, bispecific T cell engager) 후보물질이 등장했다. BiTE는 암 항원과 T세포 수용체에 동시에 결합하는 이중항체로, T세포를 종양부위로 끌어들이는 브릿지 역할을 한다.
암젠은 최근 열린 'Myeloma 2018'에서 재발/불응성 다발성골수종 환자를 대상으로 임상 1상을 진행하고 있는 BCMA X CD3 BiTE 'AMG 420'의 초기 임상 1상 데이터를 발표했다. 암젠은 고용량 투여군에서 5명의 환자가 엄격한 완전관해(sCR, stringent complete responses)를 보였다고 밝혔다. sCR은 완전관해(CR)보다 더 높은 치료율을 말하는 기준이다. 다발성골수종 환자에서 약물 투여에 따른 반응은 sCR/CR/VGPR(very good partial response)/부분반응(PR)/안정병변(SD) 순서로 높다.
주목할 점으로 이중 4명의 환자가 미세잔존질환 음성(MRD (-), minimal residual disease negative) 단계에 돌입했다. 환자가 미세잔존질환 음성이라는 것은 100만 개의 골수세포(bone marrow cells)에 1개 미만의 골수종 세포(myeloma cell)가 남아있다는 뜻이다. 질환이 검출되지 않다는 의미로, 재발 위험이 낮은 상태다. 또한 5명 중 4명의 환자에서 10개월 이상 반응이 지속됐다. 사이토크롬신드롬(CRS) 부작용도 모두 1등급에 그쳐, 안전성 이슈는 없었다.
AMG 420의 초기 임상 데이터가 발표되고, BCMA CAR-T 선두주자인 셀진/블루버드의 'bb2121'에 뒤지지 않는다는 긍정적인 평가가 나왔다. 즉 다발성골수종 시장을 겨냥한 BCMA 약물의 새로운 경쟁구도가 형성되고 있는 것. 임상 1상에서 22명의 재발/불응성 환자를 대상으로 bb2121을 투여(150x10^6)했을 때, 50% CR/sCR, 36.4% VGPR, 95.5% 전체 반응률(ORR)을 보였다. 반응 기간의 중간값은 10.8개월이었다.... <계속>