기업
대웅·종근당, 새 먹거리 발굴 '분주'..작년 임상 최다
바이오스펙테이터 천승현 기자
식약처, 2016년 임상시험 승인현황 분석..대웅-복합제ㆍ종근당-신약 개발 뚜렷
지난해 국내 제약기업 중 대웅제약과 종근당이 가장 많은 의약품 임상시험에 착수한 것으로 나타났다. 새 먹거리 발굴을 위해 가장 분주한 행보를 나타냈다. 바이오업체 중에서는 강스템바이오, 셀트리온, 제넥신 등이 눈에 띄는 개발 활동을 보였다.
11일 식품의약품안전처에 따르면 지난해 승인받은 의약품 임상시험 계획은 총 627건으로 집계됐다. 지난해 1년 동안 국내제약사, 다국적제약사, 연구기관, 임상수탁기관 등이 총 627건의 임상시험을 시작했다는 의미다. 2015년 675건보다 7.1% 감소한 수치다.
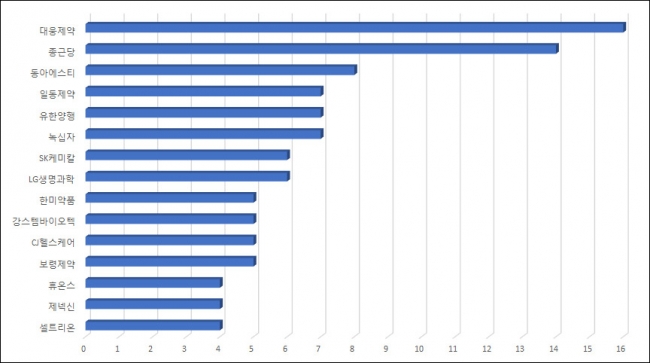
▲2016년 주요 국내기업 임상시험 승인 건수(단위: 건, 자료: 식품의약품안전처)
이 중 국내기업이 승인받은 임상시험은 191건으로 전체의 28.3%를 차지했다. 국내제약사와 바이오기업의 신약·개량신약 개발 활동을 짚어보기 위해 국내기업의 임상시험 승인 자료만 분석해봤다. 임상시험 계획의 승인 건수가 기업들의 R&D 능력이나 의지를 반영하는 수치는 아니지만 새롭게 임상시험에 착수하는 과제를 통해 제약사들의 미래 먹거리 발굴 현황을 들여다보기 위해서다.
업체별로는 대웅제약이 지난해 가장 많은 16건의 임상시험에 착수했다. 2015년 7건보다 2배 이상 많은 임상시험을 시작했다. 대웅제약은 지난 2012년부터 2015년까지 4년간 17건의 임상시험 계획을 승인받았는데, 최근 들어 새로운 의약품의 개발에 속도를 내고 있다는 뜻이다.
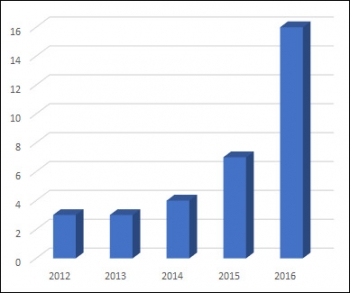
▲연도별 대웅제약 임상시험 계획 승인 건수
대웅제약이 지난해 착수한 16건의 임상시험 중 11건이 임상1상 단계로 나타났다. 신약 개발 초기 단계의 제품이 많다는 의미다.
대웅제약이 지난해 착수한 임상시험 과제를 보면 복합제 개발에 역점을 두는 듯한 인상이다. 지난해 승인받은 16건의 임상시험 중 10건 이상은 2개 이상의 약물을 결합한 복합제 관련 임상시험으로 조사됐다. 2개의 고혈압약(올메사르탄, 암로디핀)과 고지혈증약(로수바스타틴)을 결합한 3개의 약으로 구성된 복합제도 막바지 임상시험을 진행 중이다. 보툴리눔제제 ‘나보타’의 적응증 확대를 위한 임상시험도 2건 승인받았다.
종근당이 지난해 14개의 임상시험에 돌입하며 뒤를 이었다. 대웅제약과 종근당이 총 30개의 임상시험 계획을 승인받았는데, 이는 국내기업이 지난해 승인받은 임상시험 계획의 15.7%의 해당한다.
종근당은 다양한 파이프라인을 가동했다. 고지혈증약(CKD-519), 림프종치료제(CKD-581) 등 신약 개발에 왕성한 행보를 나타냈고, 당뇨복합제(CKD-395), 고지혈증복합제(CKD-391), 당뇨복합제(CKD-396) 등 복합제 개발에도 속도를 냈다. B형간염치료제 ‘비리어드’의 제네릭 개발을 위한 임상시험(CKD-390)에도 뛰어들었다.
동아에스티(8건), 일동제약(7건), 유한양행(7건), 녹십자(7건) 등이 새로운 임상시험 시도 사례가 많았다.
한미약품은 5건으로 대형 제약사 중 상대적으로 임상시험 계획 승인 건수가 적었는데 이미 기술수출한 신약들은 국내보다는 글로벌 임상시험을 진행 중이고, 새로운 신약 과제보다는 기존 과제의 상업화 작업에 더 역점을 둔 것으로 분석된다.
바이오업체 중에서는 강스템바이오텍이 지난해 5건의 임상시험에 돌입하며 상위권에 랭크됐다. 강스템바이오텍은 제대혈 유래 동종줄기세포치료제 ‘퓨어스템’ 개발을 위한 임상시험만 4건 진입했다. 퓨어스템을 류마티스관절염치료제, 만성아토피피부염치료제 등으로 개발하기 위한 작업이다.
셀트리온과 제넥신도 각각 4건의 임상시험에 착수하며 대형 제약사보다도 활발한 개발활동을 보였다. 셀트리온은 항체바이오시밀러 램시마의 피하주사제(CT-P13)와 독감치료용 항체물질(CT-P27) 개발을 진행했다. 제넥신은 지속형 성장호르몬 등의 임상시험에 돌입했다.
한편 지난해 임상시험시험 계획을 1건이라도 승인받은 국내 기업은 총 81곳으로 집계됐다. 식약처에 따르면 2015년 기준 완제의약품 생산업체는 356곳에 달한다.
국내 완제의약품 업체 4곳 중 1곳만이 지난해 신약과 개량신약 개발을 위한 새로운 임상시험을 시도했다는 의미다. 반대로 4곳 중 3곳은 자체개발 신약 및 개량신약 보다는 임상시험이 필요없는 제네릭이나 일반의약품 허가·판매에 주력한 것으로 풀이된다.



















