기업
면역항암 효과 IL-2 돌연변이 물질, 개발 파트너 찾는다
바이오스펙테이터 조정민 기자
[쿠바 바이오파마 기술 소개②]쿠바 분자면역학센터(CMI) 개발, 전임상 단계 IL-2 변형단백질
암을 정복하고자 하는 의료진과 연구자들은 다양한 기전을 이용한 연구를 계속하고 있다. 최근 가장 활발히 연구 중인 항암 치료법은 체내의 면역 시스템을 이용해 암세포를 제거하는 것으로, 이미 다양한 면역항암제들이 개발되거나 혹은 임상을 진행하고 있다.
쿠바의 분자면역학센터(CMI)의 연구진은 T세포와 NK세포를 활성화시켜 강한 면역작용을 유도하는 인터루킨-2(Interleukin 2; IL-2)에 주목했다. IL-2는 T세포 성장인자로도 불리며, 작동 T세포(Effector T cell)과 조절 T세포(Regulatory T cell)를 이중으로 활성화함으로써 면역 반응을 조절하는 역할을 수행한다. IL-2는 보조 T세포(T helper cell)의 세포막에 존재하는 인터루킨-2 수용체(Interleukin-2 Receptor; IL-2R)에 결합해 T세포의 분화 방향을 결정하게 된다.
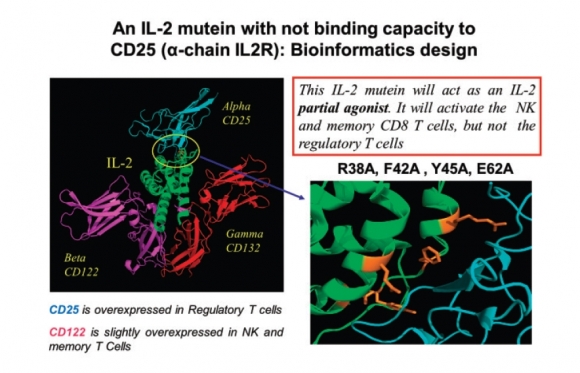
IL-2 수용체는 α, β, γ 3개의 폴리펩타이드 체인으로 구성돼 있으며 각 면역세포 별로 수용체의 체인이 다르게 발현한다. 예를 들면 조절 T세포에는 수용체 α체인 발현이 높게 나타난다.
면역조절 세포치료제의 원조라고 할 수 있는 림포카인 활성세포 치료의 경우, IL-2의 면역세포 조절기능을 바탕으로 환자에게서 얻은 림프구를 고농도의 IL-2와 같이 배양해 항암면역기능을 증가시킨 것이다. 하지만 고농도의 IL-2 적용 치료는 면역 관문 억제반응이 동시에 나타나 만족스러운 효과를 보이지 못했다.
연구진은 IL-2 고농도 항암 요법과 비교해 높은 치료적 효과를 볼 수 있는 방법을 찾기 위해 연구를 거듭한 끝에 IL-2 수용체의 α 또는 γ 체인에 결합하는 부분을 변이시킨 2 종의 IL-2 돌연변이 단백질을 개발했다. 면역세포 별로 IL-2 수용체 구성 체인이 다르게 나타나는 것에서 착안, 선택적으로 결합을 방해함으로써 해당 면역 세포 활성화를 억제하는 기전이다.
IL-2 수용체 α체인인 CD25 단백질에 결합하는 부분을 변이시켜 결합이 발생하지 않도록 하는 'No alpha IL-2'는 조절 T세포에서 많이 발현되는 α체인에는 결합하지 못하고, CD8+ 기억 T 세포와 자연살해세포(NK cell)이 많이 발현하는 β, γ 체인에만 결합함으로써 면역반응을 활성화시킨다.
흑색종 마우스 모델 실험에서 'No alpha IL-2' 적용군의 종양의 크기가 식염수(대조군)과 기존의 IL-2 적용군과 비교해 유의미하게 줄어들었으며, 높은 전이 억제 효과를 나타내는 것을 확인했다.
연구진은 IL-2 수용체 γ체인 결합부를 변이시킨 'No gamma IL-2'도 개발했다. γ체인은 IL-2가 수용체에 결합하는데 아주 중요한 역할을 수행하는 것으로 알려졌다. 따라서 γ체인 결합부에 변이가 발생하면 IL-2의 결합이 억제되고 우선적으로 조절 T세포로의 분화가 줄어들게 된다는 설명이다. 이 또한 동물모델에 적용했을 때, 항암효과가 증가하는 것을 확인했다고 밝혔다.
쿠바 연구진은 현재 두 가지 돌연변이 단백질에 대한 전임상을 수행하고 있다. 오는 9월 12일 서울울 양재동 엘타워에서 열리는 '한-쿠바 바이오파마 기술교류 세미나'에서 개발과 제품화를 공동으로 진행할 파트너를 찾을 계획이다.
[한-쿠바 바이오파마 기술교류 세미나]
• 일시: 2017년 9월 12일(화) 14시
• 장소: 서울 양재 엘타워 골드홀(지하1층)
• 주최: 한국바이오의약품협회, 바이오스펙테이터
• 후원: 싸토리우스코리아
















