기업
액섬, '다중기전' 경구용 급성편두통 장기3상 “통증 완화”
바이오스펙테이터 서윤석 기자
CGRP 방출 억제, 신경염증, 통증신호전달 억제 ‘AXS-07’..3상서 2시간내 환자 68% 통증완화 및 47% 성가신증상 제거..1분기 신약허가신청(NDA) 예정

액섬(Axsome Therapeutics)가 다중기전을 가진 경구용 약물 'AXS-07'의 급성 편두통 대상 장기 임상 3상에서 통증완화 효과와 안전성을 확인한 결과를 내놨다. 액섬은 이런 결과를 바탕으로 1분기에 신약허가신청(NDA)을 제출할 예정이다.
액섬은 지난달 31일(현지시간) 급성 편두통(migraine) 치료제 후보물질 ‘AXS-07’의 12개월간 진행한 장기 임상 3상(Movement study, NCT04068051)에서 투여 2시간내 68%의 환자에서 통증을 완화하고 안전성을 확인한 긍정적인 결과를 발표했다.
액섬의 급성 편두통 치료제 후보물질 AXS-07(20mg meloxicam+10mg rizatriptan)은 경구용 약물로 CGRP 방출을 억제하고, 신경염증, 통증신호 전달을 억제함으로써 작용하는 기전이다.
발표에 따르면, 액섬은 706명의 급성편두통 환자를 모집해 12개월간 임상을 진행했다. 급성 편두통 환자들은 AXS-07 투여 1시간내 39%(37~41%), 2시간내 68%(65~71%)가 통증완화(pain relief)를 나타냈다. 또, AXS-07을 투여받은 환자들은 2시간내 47%(46~49%)에서 대부분의 성가신증상(most bothersome symptom, MBS)이 사라졌다.
AXS-07을 투여한 환자의 통증완화 지속비율(rates of sustained pain relief)은 2~24시간 동안 60%(59~62%), 2~48시간 동안 59%(58~60%)를 나타냈다. 또, AXS-07을 투여한 환자의 통증해소 지속비율(rates of sustained pain freedom)은 2~24시간, 2~48시간 동안 각각 33%(33~35%), 32%(32~34%)였다.
액섬은 AXS-07이 12개월간의 장기간 복용에서 안전성을 확인했다. 가장 일반적인 이상반응은 메스꺼움, 현기증, 구토 등이었으며, 1.6%의 환자는 부작용으로 임상을 중단했다.
액섬은 지난해 4월 302명의 급성편두통 환자를 대상으로 진행한 임상 3상(Intercept study, NCT04163185)에서 2시간내 통증 해소(pain freedom)와 대부분의 성가신증상(MBS)을 각각 32.6%(vs 16.3%, p=0.002), 43.9%(vs 26.7%, p=0.003)으로 유의미하게 완화시킨 결과를 밝혔다. 또, AXS-07을 투여했을 때 위약보다 신속한 통증감소 효과를 나타낸 바 있다.
Herriot Tabuteau 액섬 CEO는 “이번 임상결과는 AXS-07의 효능과 장기 안전성 프로파일을 보여준다”며 “이번 결과를 기반으로 올해 1분기에 AXS-07를 급성 편두통에 대해 신약허가신청(NDA)을 제출할 것”이라고 말했다.
한편, 액섬은 NMDA 수용체 길항제 'AXS-05'의 알츠하이머병 초조증 임상 2/3상과 주요우울장애(MDD) 임상 3상에서 긍정적인 결과를 발표한 바 있다.
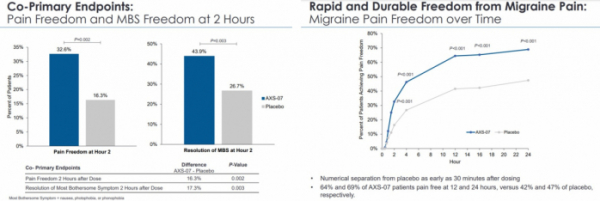
▲AXS-07 인터셉트 임상 3상 결과(액섬 발표자료 참조)