기업
올릭스, ‘CTGF asiRNA’ 비대흉터 美2a상 “탑라인”
바이오스펙테이터 서윤석 기자
CTGF asiRNA ‘OLX101A’, 24주시점 비대흉터 재발지표 POSAS 점수 3.3, 위약군 3.8점

올릭스(OliX Pharmaceuticals)는 27일 CTGF asiRNA 후보물질 ‘OLX101A(OLX10010)’의 비대흉터 미국 임상2a상(NCT04877756)의 탑라인 결과를 공시했다.
공시에 따르면 올릭스는 흉터재건술을 시행한 환자 20명을 저용량군과 고용량군으로 각각 10명씩 나눠 흉터재건술 부위 절반은 약물을, 절반은 위약을 투여했다. 1차종결점은 흉터재건술 후 약물 투약 24주시점에서 POSAS 점수(Patient and Observer Scar Assessment Scale overall opinion score를 이용해 비대흉터 재발정도를 비교하는 것으로 설정했다. 1차종결점 측정방법은 기준선(baseline) 흉터의 시각적, 촉각적 특성의 전반적인 심각도를 1~10까지 측정한 후, 24주차시점에 동일 흉터를 재측정해 흉터의 개선정도를 수치로 분석했다. POSAS 점수는 낮을수록 정상에 가깝다는 의미다.
그 결과 24주차시점에서 OLX101A를 투여한 평균 POSAS 점수는 투약군 3.3점으로 기준선 대비 1.8점 감소해 통계적으로 유의미한 차이를 보였다(p<0.017). 위약군은 3.8점으로 기준선 대비 1.2점 감소하는 경향을 보였다(p=0.065). 24주차 시점에서 OLX101A 투여군과 위약군간 비교한 결과는 공개하지 않았다.
올릭스는 향후 48주차 시점의 안전성 평가 등 2차종결점에 대한 결과가 포함된 임상결과보고서(CSR)를 수령할 예정이다.
비대흉터의 섬유화 과정에서 CTGF(Connective tissue growth factor)는 중요한 인자로 알려져 있으며, 현재까지 적절한 비대흉터 치료제는 없는 상황이다. OLX101A는 CTGF를 타깃하는 asiRNA 후보물질이다.
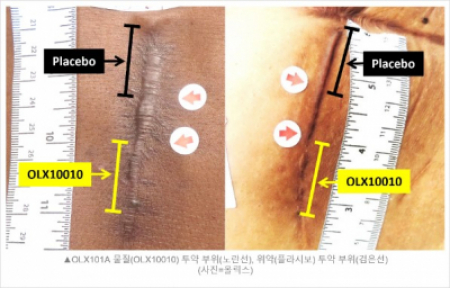
(올릭스 제공)