국제
아큘-다이이찌산쿄, MET 표적항암제 3상 실패.."다시 제자리"
바이오스펙테이터 김성민 기자
'블록버스터 가능성' 글로벌 제약사들 계속된 도전...국내 에이비온, MET 겨냥 항체 개발 "독성부작용 개선약물로 임상계획"

MET을 겨냥한 표적항암제가 또 다시 실패로 돌아갔다. 아큘(ArQule)과 다이이찌산쿄(Daiichi Sankyo)가 공동개발하던 MET 표적항암제 '티반티닙'이 이차치료제로 간세포암종(HCC, hepatocellular carcinoma) 환자에서 진행하던 임상3상에서 실패했다고 17일 밝혔다.
티반티닙((tivantinib, ARQ197)은 METIV-HCC trial에서 일차 충족점인 전체생존기간(OS, overall survival)을 연장하지 못했다. 이차 충족점의 기준은 무진행생존기간(PFS, progression-free survival)과 안전성으로, 추가적인 데이터는 이후 과학 컨퍼런스에서 발표하겠다고 전했다.
MET은 주로 위암, 대장암, 간암 등을 포함한 고형암에서 과발현, 암 진행과 전이, 내성에 관여하는 대표적인 유전자다. 기전상의 중요성 때문에 EGFR(상피세포 성장인자수용체)의 활성변이 다음으로 암에서 활발하게 연구됐지만, 아직 MET을 겨냥해 승인받은 치료제가 없다. 2014년 로슈 오나투주맙(onartuzumab) 임상3상 실패를 포함한 글로벌 제약사의 수많은 시도에도 불구하고 임상에서 번번이 고배를 마신 것. 그러나 시판될 될 경우 블록버스터 제품이 가능하기에 티반티닙의 이번 임상결과에 눈길이 쏠려있었다.
티바티닙은 이전에도 비소세포폐암에서 임상실패를 경험했던 약물이다. 2012년 비소세포폐암에서 일차 충족점인 OS를 도달하지 못해 임상을 중단한 이후, 추가적인 약물기전 데이터를 확보해 HCC 환자에서 2013년에 다시 임상을 재개한 것으로 FDA, EMA로부터 희귀의약품 지정을 받은 바 있다.
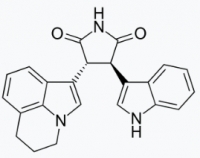
▲티바티닙 구조위키피디아 참조
티바티닙은 경구용 MET 특이적 억제제로, IC50 값(약물이 50% 억제효율을 나타내는 농도)은 0.1uM이다. 이번 임상은 340명의 MET 과발현한 환자를 대상으로 진행된 것으로 면역조직화학 어세이를 통해 환자를 스크리닝했다. 임상에서 실패했던 경험을 바탕으로 성공확률을 높이기 위해 바이오마커를 사용한 것이다.
Paolo Pucci 아큘 CEO는 "HCC 환자의 이차치료제는 미충족 의료수요가 매우 큰 부분으로, 이번 임상결과는 환자와 기업에게 실망감을 안겨줬다"고 말했다. 회사는 이외에도 FGFR 억제제, 2개의 pan-AKT 억제제 표적항암제 파이프라인을 진행중이다.
글로벌 시장에서 아직 MET을 겨냥한 항체, 표적항암제 등의 임상이 진행중이다. 대표적인 예로 아스트라제네카 볼루티닙(Volitinib), 에자이 골바티닙(Golvatinib) 등이 있다.
한편, 국내에서도 MET 억제제에 도전하는 기업이 있다. 에이비온(Abion)은 2014년 화학연구원이 가진 'c-met 억제제'의 우수한 특이성(selectivity)을 보고 라이선스 인을 해, 신장독성이 없는 형태로 개발했다. 신장독성은 이전 임상에서 실패한 주요원인 중 하나로 꼽힌다. ABN 401는 유전자증폭(amplication), 엑손결실, c-met 돌연변이 등의 바이오마커를 이용해 위암환자에서 우선적으로 글로벌 임상을 진행할 계획이다.

















