국제
타우역할 뒤엎는 연구결과..“타깃약물, AD 악화할수도"
바이오스펙테이터 김성민 기자
美드렉셀 연구진, 타우 미세소관 안정화 아닌 '역동성' 갖게하는 요소라고 주장, MAP6 미세소관 안정화 기여..."퇴행성뇌질환 환자 뇌 미세소관 역동성 잃어버리는 것이 문제, 타우 등 미세소관 안정화 타깃 신약후보물질 의문 제기"
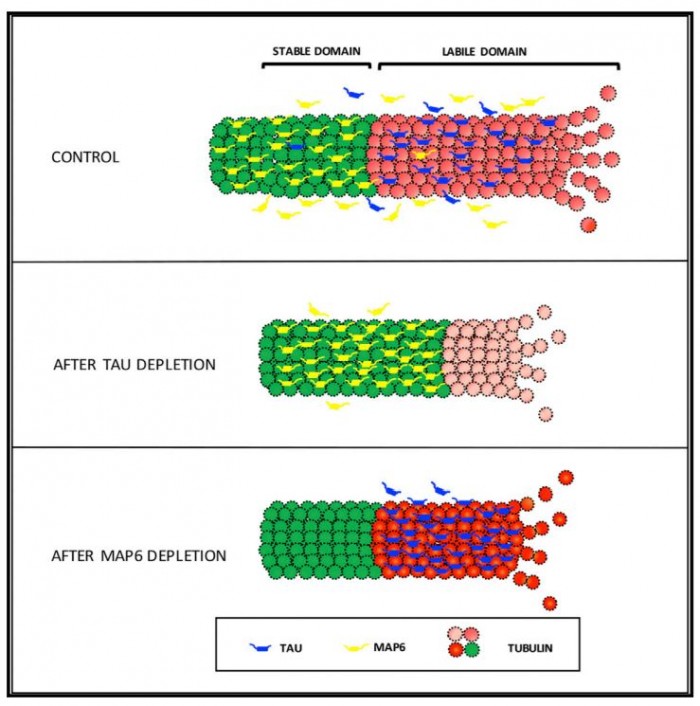
▲'Tau Does Not Stabilize Axonal Microtubules but Rather Enables Them to Have Long Labile Domains'라는 제목의 논문의 그래픽 초록, doi: 10.1016/j.cub.2018.05.045
'타우(Tau)'에 대한 새로운 견해가 발표돼 논란이 일고있다. 타우는 알츠하이머병을 일으키는 주요인자다. 환자의 뇌에서 미세소관을 안정화하는 타우가 인산화됨에 따라 미세소관에서 떨어져나오고, 구조가 망가지면서 신경엄킴(neurofibrillary tangles)이 형성된다. 따라서 신경세포내의 원활한 물질수송 및 신호전달이 저해되면서 세포사멸에 이르게 된다. 이것이 알츠하이머병 환자 뇌에서 일어나는 일이다. 이에 병리진행에 작용하는 타우를 타깃하거나 혹은 미세소관을 안정화하는 것이 현재 개발중인 신약 후보물질이 가진 접근법이다.
그런데 미국 드렉셀(Drexel) 대학 연구진이 기존에 알려진 타우의 역할과 반대되는 이론을 뒷받침하는 연구결과를 발표했다. 내용의 골자는 타우가 미세소관을 안정화하는게 아니라 오히려 미세소관이 성장할 여지를 갖게하는 역동성(dynamics)을 부여하는 요소라는 것. 미세소관은 크게 안정화 도메인(stable domain)과 불안정한 도메인(labile domain)으로 나뉜다. 불안정한 도메인에서 미세소관이 길어질 수 있는 역동성을 가진다.
연구결과는 '타우는 엑손 미세소관을 안정화하기 보다는 불안정한 도메인을 가지게 돕는다(Tau Does Not Stabilize Axonal Microtubules but Rather Enables Them to Have Long Labile Domains)'라는 제목의 논문을 셀(Cell)의 자매지인 'Current Biology'에 지난 28일 게재했다.
연구를 주도한 드렉셀대의 Peter Baas 박사는 "미세소관이 '안정성'을 잃어버리면서 알츠하이머병이 발병한다는 것이 주류이론"이라며 "반면 우리의 이번 연구는 타우가 고갈되면서 오히려 알츠하이머병 환자 뇌에서 미세소관이 '역동성'을 잃어버리는 것이 문제가 된다는 것을 보여준다"고 강조했다.
드렉셀 연구팀의 주장에 따르면 알츠하이머병 환자의 뇌에서 필요한 것은 미세소관의 안정성이 아닌, 역동성이라는 것이다. Baas 박사는 "타우 타깃 후보물질을 포함해 미세소관을 안정화하는 약물(microtubule-stabilizing drugs)은 오히려 알츠하이머병의 병기진행을 악화할 가능성이 있는 것"이라며 임상개발 중인 신약후보물질에 대한 의문을 제기했다.
타우는 차세대 알츠하이머병 타깃으로 퇴행성뇌질환에 포커스하는 빅파마는 타우 타깃 에셋을 사들였거나 혹은 자체적으로 개발하고 있다. 빅파마로 애브비, 셀진, 바이오젠, 머크, 다케다, BMS, 릴리 등이 타우 프로젝트를 진행하고 있다.
이번 논문에서 연구진은 배양한 랫드 뉴런(cultured rat neurons)에서 타우를 고갈한 4일후 미세소관 부피가 줄어들어든 것을 관찰했다. 그러나 타우가 없어지면서 미세소관이 분리된 것이 아니라 미세소관의 역동성이 줄어들고, 이에따라 미세소관의 길이가 짧아지면서 나타난 현상이라는 설명이다. Baas 교수는 "실제 뉴런에서 타우는 미세소관의 길이를 늘리는 역할을 했다"며 "철길을 묶기 보다는 다리의 교각처럼 미세소관을 연장하기 위해 규칙적으로 필요한 요소"라고 강조했다.
그러면 실제 미세소관을 안정화하는 인자는 뭘까? 연구팀은 MAP6(microtubule-associated protein 6)를 제시했다. 뉴런에서 타우가 고갈되게 되면 MAP6가 퍼지면서 오히려 미세소관이 더욱 안정화되는 개념이다. 연구팀은 향후 성인 설치류 뇌에서 이러한 개념을 입증할 계획이다.


















