국제
젠사이트, LHON 유전자 치료 임상3상 “시력 개선”
바이오스펙테이터 이승환 기자
미토콘드리아 DNA에 G11778A 돌연변이 가진 ND4 레버씨 유전성 시신경병증(LHON)..AAV2 기반 유전자 치료 후보물질 ‘GS010’ 투여해 시력 개선 확인

망막 신경 퇴행 질환, 중추신경계 질환에 대한 유전자 치료제를 개발하는 프랑스 젠사이트 바이오로직스(GenSight Biologics)가 레버씨 유전성 시신경병증(Leber Hereditary Optic Neuropathy, LHON) 유전자 치료 후보물질 ‘GS010(rAAV2/2-ND4)’를 96주간 투여한 임상3상(RESCUE, NCT02652767) 결과를 지난 23일(현지시간) 발표했다.
레버씨 유전성 시신경병증은 미국과 유럽을 통틀어 매년 1400~1500여 명의 환자가 시신경의 위축으로 인해 시력을 상실하는 희귀한 질환이다. 보통 20~30대에 첫 증상이 나타나는 것으로 알려졌지만, 통증 없이 급성으로 시력저하가 나타나기 때문에 발병 시기에 대한 환자 간 격차는 크다. 첫 증상을 확인한 이후 12개월 이내에 시력 정확도가 급격하게 낮아져 실명한 수준에 이른다.

▲시력 정확도 저하 예시(젠사이트 발표자료)
RESCUE 연구는 증상이 6개월 이내에 나타난 레버씨 유전성 시신경병증 환자를 대상으로 진행했다. 젠사이트는 레버씨 유전성 시신경병증 환자 가운데 미토콘드리아 DNA(mitochondrial DNA, mDNA)에 G11778A 점돌연변이를 가진 39명을 대상으로 RESCUE 연구를 진행했다.
젠사이트는 RESCUE 연구에 참여한 39명의 환자 모두에게 GS010 투여와 가짜(sham) 투여를 동시에 진행했다. 무작위로 선정된 한쪽 안구에는 GS010을 유리체 안에 투여했으며, 다른 쪽 안구에는 바늘이 없는 뭉툭한 주사기를 이용해 유리체 내 투여 시 발생하는 압력만 가하는 방식으로 가짜 투여했다. 젠사이트는 GS010 투여, 가짜 투여를 1회 진행한 이후, 96주간 환자 시력 정확도의 변화를 추적했다. 시력 정확도는 LogMAR로 측정됐다. 0.0 LogMAR는 정상시력 1.0을 말하며, 양수 LogMAR는 정상시력 이하의 낮은 시력, 음수 LogMAR는 정상시력 이상의 높은 시력을 의미한다. 1.3 LogMAR를 넘으면 시력 정확도가 낮아 실명한 것으로 판단한다.
RESCUE 연구에서 약물 투여 이후 측정한 가장 낮은 수준의 최대교정시력(Best Corrected Visual Acuity, BCVA)을 기준으로 시력 정확도 변화를 확인했을 때, 0.498 LogMAR가 감소한 수준의 시력 개선이 나타났다고 젠사이트는 밝혔다. 0.1 LogMAR 차이는 ETDRS 시력표에서 한 줄(5글자) 차이를 의미하는데, 0.498 LogMAR는 24.9글자에 해당하는 수치다. 이는 ETDRS 시력표에서 5줄 차이의 글자를 읽을 수 있는 수준이다.
ETDRS 시력표를 기준으로 GS010을 투여받은 안구가 읽을 수 있는 평균 글자 수는 48주차 12.8글자(SD: 17.9), 72주차 20.6글자(SD: 26.3), 96주차 24.9글자(SD: 3.8)가 증가했다. 가짜 투여 안구가 읽을 수 있는 평균 글자 수는 48주차 11.8글자(SD: 15.6), 72주차 21.7글자(SD: 25.1), 96주차 22.3글자(SD: 3.8)가 증가한 것으로 나타났다. GS010 투여 안구와 가짜 투여 안구 간의 유의미한 차이가 있는지는 공개되지 않았다.
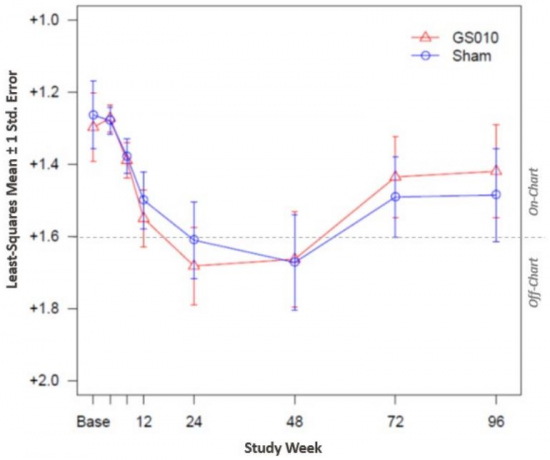
▲RESCUE 연구, 시간대별 최대교정시력의 LogMar 변화(젠사이트 발표자료)
레버씨 유전성 시신경병증 환자에게서 시신경 위축이 일어나는 원인은 정확히 밝혀지지 않았다. 시신경 위축이 나타난 95%의 환자에게서 미토콘드리아 DNA에 G11778A, G3460A, T14484C 총 3가지의 점돌연변이가 발견된다. MD4 미토콘드리아 유전자에 있는 G11778A 점돌연변이는 북유럽 환자의 70%, 아시아 환자의 90%에게서 발견되는 것으로 알려졌다. 그러나 돌연변이를 가진 남성의 50%, 여성의 85% 이상은 시력상실이나 유사 증상이 나타나지 않기 때문에 확실한 인과관계는 확인되지 않았다. 현재는 점돌연변이로 비정상적인 에너지 생산과정을 보이는 미토콘드리아가 시신경 위축의 원인으로 추정한다.
젠사이트가 개발한 GS010은 아데노 연관 바이러스(adeno-associated virus vector, AAV) 벡터2(vector 2)를 이용한 유전자 치료 후보물질이다. GS010은 레버씨 유전성 시신경병증 환자의 미토콘드리아에 G11778A 점돌연변이가 없는 정상 유전자를 집어넣는다. 이를 통해 정상적인 단백질을 합성할 수 있게 된 미토콘드리아는 에너지 생산과정이 정상으로 회복돼 시신경 위축을 일으키지 않는다고 젠사이트는 설명한다.


















