기업
'NASH신약 도전' 美 인터셉트 "3상 중간결과 1Q 공개"
바이오스펙테이터 장종원 기자
[JPM 2019]진행중인 ‘REGENERATE’ 3상 Top-line 데이터 공개 예정..적응증 확대 위해 새 임상 착수

비알코올성 지방간염(NASH) 치료제 시장의 첫 깃발은 누가 꼽을 것인가. 인터셉트 파마슈티컬즈(Intercept pharmaceuticals), 길리어드(Gilead), 장피트(Genfit), 앨러간(Allergan) 등이 NASH 임상 3상에 속도를 내고 있다.
미국 뉴욕의 신약개발기업 인터셉트는 9일(현지시간) 미국 샌프란시스코에서 개최된 ‘JP모건 헬스케어 컨퍼런스’에서 NASH 치료제 ‘OCA(Obeticholic acied)’의 개발 진행 상황에 대해 발표했다.
마크 프루잔스키(Mark Pruzanski) 인터셉트 CEO는 “올해 1분기 안에 진행 중인 OCA 임상 3상 ‘REGENERATE’의 중간 분석 결과의 주요 데이터(top-line data)를 공개할 것"이라면서 "또한 보상적 간경변이 발생한 NASH 환자까지 적용대상을 확장하기 위한 새로운 임상3상 ‘REVERSE’를 진행할 것”이라고 말했다.
인터셉트는 담즙산 생합성을 조절하는 핵 내 수용체 FXR(Farnesolid X recepter)의 활성을 유발하는 OCA를 NASH 치료제로 개발하고 있다. 답즙산, 당, 지방 대사와 염증 및 섬유화를 조절하는 것으로 알려진 FXR을 타깃해 간세포의 지방 축적을 억제하고 에너지 고갈로 인한 세포 사멸을 방지한다는 전략이다. 해당물질은 2016년 ‘원발성 담즙성 담관염(primary biliary cholangitis; PBC)의 2차 치료제로 승인받은 바 있다.
조직학적으로 증명된 NASH 환자 283명을 대상으로 72주간 진행된 OCA 임상 2상(FLINT)에서 OCA는 NASH의 조직학적 마커와 섬유화 수치를 유의미하게 호전시킨 것이 확인됐다. 위약군과 OCA 25mg 적용군을 비교했을 때, OCA 적용군의 NAS 평가지표가 모두 개선됐고, 간의 섬유화(fibrosis)와 지방증(steatosis), 염증, 세포변형 정도와 간 기능 관련 생체 지표도 호전되는 것을 확인했다.

해당 임상연구 결과가 게재된 국제 학술지 ‘란셋(The Lancet)’을 살펴보면 1단계 이상 섬유화가 개선된 환자의 경우, 위약군은 19%인 반면 OCA 적용군은 35%로 확인됐다. 이러한 결과는 OCA가 간 섬유화를 유의미하게 개선하는 첫 번째 약물로 인정받아 미국 FDA로부터 혁신 신약으로 지정되는 근거로 작용했다.
2~3단계의 섬유화(F2~F3)에 해당하는 환자로 범위를 좁힌 사후 검증 분석에서는 위약군(21%)와 비교해 약 20% 상승한 40%의 환자가 섬유화가 개선된 것으로 분석됐다. 전체 모집단 분석에서는 유의미한 통계적 차이를 보이지 않았던 이차종결점 평가기준인 ‘섬유화 악화 없는 NASH 개선(NASH resolution)’도 사후 검증에서는 위약군(7%)과 비교해 유의미하게 증가했다(OCA 적용군 20%).
인터셉트는 현재 2~3단계의 섬유화가 발생한 NASH 환자 2300명을 대상으로 위약과 OCA 10mg, 25mg을 72주간 투약하고 섬유화 개선과 NASH 증상 개선을 확인하는 임상 3상 ‘REGENERATE’를 진행하고 있다. 회사 측은 750명 이상의 환자 결과를 분석한 중간 분석 최초 데이터를 2019년 1분기 내에 공개할 것이라고 밝혔다.
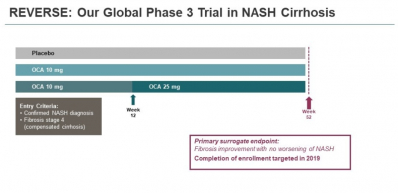
또한 인터셉트는 OCA의 적응증 확장을 위해 보상성 간경변이 동반된 중증 NASH환자를 대상으로 OCA의 효능을 확인하는 새로운 임상3상(REVERSE)을 설계하고 현재 환자를 모집하고 있다.
540명 규모로 설계된 REVERSE 임상은 4단계의 섬유화와 보상성 간경변이 발생한 중증의 NASH 환자를 대상으로 위약 대비 OCA의 효능을 평가한다. 일차종결점은 NASH의 악화 없이 1단계 이상 섬유화가 개선되는 것이며, NASH 임상연구 네트워크(Clinical Research Network; CRN) 점수 체계를 이용해 평가, 분한다. 이차종결점으로는 2단계 이상의 섬유화 개선과 NASH 증상 개선 등이 설정됐다. 마크 프루잔스키 대표는 “2019년 안에 해당 임상의 환자 모집을 완료하는 것을 목표로 진행 중이다”라고 말했다.



















