피플
KRIBB 김장환센터장, ‘직접분화 줄기세포’ PD신약 개발
바이오스펙테이터 서윤석 기자
[제12회 바이오파마 테크콘서트] 파킨슨병 환자 섬유아세포서 직접분화시킨 줄기세포 ‘hiDP’..동물서 안전성 확인, 파킨슨병 증상 개선, 뇌 내 도파민 신경세포 재생효과 보여

파킨슨병 환자의 섬유아세포를 직접교차분화법(direct reprogramming)을 이용해 유도한 도파민성 신경전구세포(human induced dopaminergic neuronal progenitors, hiDP)를 적용한 파킨슨병 치료제 개발 전략이 소개됐다.
기존 유도만능줄기세포(iPSC)를 이용한 방식보다 △생산기간을 단축시키고 △도파민신경 분화능력을 높여 대량생산이 가능하고 △파킨슨병 동물모델 뇌 내 투여시 안전성과 치료효과를 확인했다는 설명이다.
김장환 한국생명공학연구원(KRIBB) 줄기세포융합연구센터장은 지난 24일 서울 한국제약바이오협회 강당에서 열린 ‘바이오파마 테크콘서트’에서 직접교차분화법을 이용한 환자맞춤형 파킨슨병 줄기세포치료제에 대해 발표했다.
파킨슨병은 65세 이상 고령화 인구에서 발병하는 대표적인 퇴행성뇌질환으로 전세계적으로 1000만명이상이 앓고 있는 것으로 알려져있다. 특히 뇌의 흑질에 있는 도파민신경이 소실되면서 발병하는 것으로 알려져 있으며 팔다리 떨림, 경직, 서행, 자세 이상 등의 운동능력 상실이 주 증상이다.
김 센터장은 “레보도파(levodopa) 등 현재 승인된 파킨슨병 치료제들은 증상을 완화시킬 뿐 질병의 근본원인인 도파민세포의 사멸을 막지 못하는 한계가 있다”며 “특히 파킨슨병은 도파민 세포를 재생시켜주면 증상이 완화되는 것으로 알려져 있어 줄기세포 치료제 등이 효과적인 것으로 알려진 질환”이라고 말했다.
대표적인 사례로 김 센터장은 태아유래 뇌조직을 파킨슨병 환자에게 이식했을 때 일부 환자에게 소실된 도파민 신경세포의 재생효과와 운동능력 개선이 확인됐으며 20년이상 이식세포의 효과가 확인된 바 있다고 소개했다. 그러나 일부 파킨슨병 환자에게서만 치료효과가 나타났으며 종양형성 등 이식세포 유래 부작용(graft induced dyskinesia)과 태아의 뇌세포를 이용한다는 윤리적인 문제가 있었다는 설명이다. 이런 태아 뇌세포, 배아줄기세포, iPSC 분화세포 등의 방식은 윤리적 문제, 종양형성가능성, 대량생산의 어려움 등 한계가 있었다.
김 센터장은 “이를 극복하기 위해 파킨슨병 환자의 섬유아세포(fibroblast)를 이용해 도파민세포를 직접분화 시킨 hiDP를 이용했다”며 “기존 만능유도줄기세포(iPSC)를 이용해 제조하는 방식보다 공정단계가 줄어들어 제조기간을 약 109일에서 63일로 약 40% 단축시킬 수 있을 뿐 아니라 파킨슨병 마우스 모델에서 hiDP의 안전성과 치료 효과를 확인했다”고 말했다.
먼저 김 센터장은 hiDP를 마우스모델의 피하에 직접 투여하고 종양원성을 확인한 결과 투여 20주가 지나도 종양형성을 확인하지 되지 않는 것을 확인했다. 대조군으로 투여한 iPSC 세포치료제는 투여 9주후부터 100% 종양이 형성된 결과를 보였다. 또 뇌에 직접 hiDP를 이식한 경우에도 종양형성은 관찰되지 않았으며 이식부위 세포의 형태도 변경되지 않아 안전성을 확인했다고 설명했다.
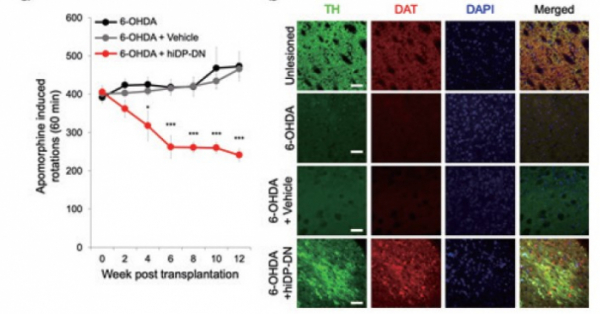
다음으로 김 센터장은 한쪽 뇌의 도파민성 신경세포를 사멸시킨 편측 파킨슨병모델에 hiDP를 투여해 치료효과를 확인했다. 편측 파킨슨병 모델에 아포모핀(apomorphine)을 투여하면 병변 반대방향으로 동물이 회전하는 증상을 보이는데, hiDP를 투여한 경우 회전운동 횟수가 유의미하게 감소한 결과를 확인했다. 특히 hiDP를 투여한 경우 도파민성 신경세포가 사멸된 뇌부위에 도파민전구체(TH)가 다시 재생되고 동물의 도파민 수치도 유의미하게 높아진 것을 확인했다.
이런 연구결과를 바탕으로 김 센터장은 “직접분화방식을 이용한 hiDP는 윤리적 문제가 없으며, 순도가 상대적으로 높고, 높은 치료효과와 이식세포유래 부작용을 해결하고, 생산성과 안전성이 높아 세포치료제로 적합할 것으로 생각한다”고 말했다.
(발표자료 참조)



















